Presencia de integrones y su correlación con la multirresistencia en Salmonella enterica serovar Typhimurium: revisión sistemática exploratoria
Resumen
La multirresistencia a los antibióticos en Salmonella enterica serovar Typhimurium (Typhimurium) se asocia con integrones que portan genes de resistencia y que son dispersados por elementos genéticos móviles.
En esta revisión sistemática exploratoria, se buscó identificar los tipos de integrones y sus genes de resistencia en aislamientos de Typhimurium multirresistentes a antibióticos. Se realizó una búsqueda de artículos en Medline, PubMed, SciELO, ScienceDirect, Redalyc y Google Académico, publicados entre el 2012 y el 2020, en español o inglés, con las palabras claves: “integrons”, “antibiotic resistance” y “Salmonella Typhimurium”. En el análisis se incluyeron 38 artículos que reportaron multirresistencia a cinco familias de antibióticos.
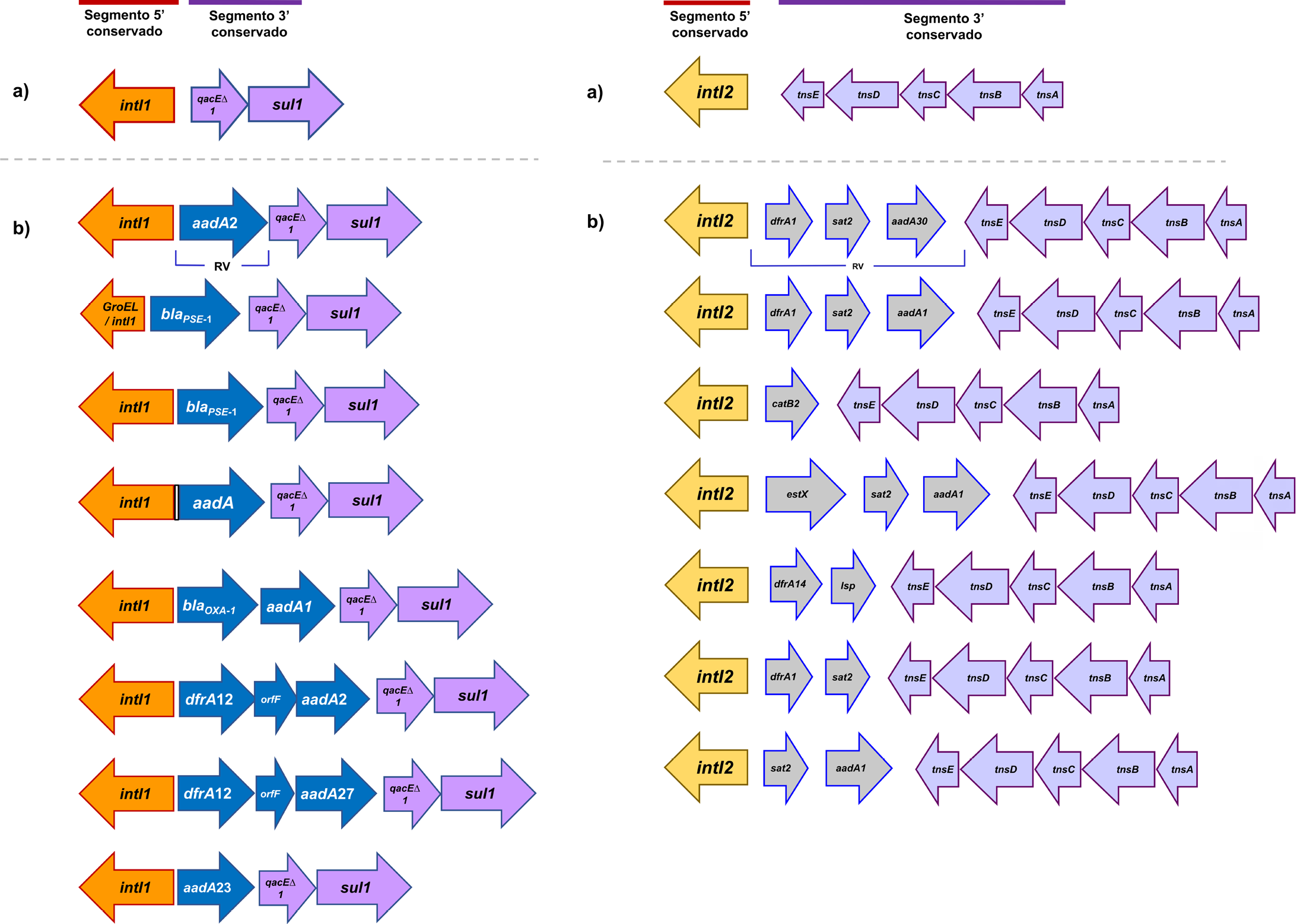
Los integrones de clase 1 con casetes de genes aadA2 y blaPSE-1 fueron los predominantes, algunos probablemente relacionados con la isla genómica de Salmonella 1. No se encontraron integrones de clase 1 y 2 en un mismo aislamiento, ni se reportaron integrones de clase 3. La presencia de integrones explica en gran medida los perfiles de resistencia encontrados en aislamientos de diferentes fuentes de 15 países.
Descargas
Referencias bibliográficas
Center for Disease Control and Prevention. CDC yellow book 2020: Health information for international travel. Brunette GW, Nemhauser JB, editors. New York: Oxford University Press; 2019. https://doi.org/10.1093/med/9780190928933.001.0001
World Health Organization, Food and Agriculture Organization of the United Nations. INFOSAN activity report 2018-2019. World Health Organization, editor. Geneva: World Health Organization; 2020. p. 76.
McQuiston JR, Herrera-Leon S, Wertheim BC, Doyle J, Fields PI, Tauxe RV, et al. Molecular phylogeny of the salmonellae: Relationships among Salmonella species and subspecies determined from four housekeeping genes and evidence of lateral gene transfer events. J Bacteriol. 2008;190:7060-7. https://doi.org/10.1128/JB.01552-07
Organización Mundial de la Salud. Salmonella (no tifoidea). 2018. Fecha de consulta: 21 de agosto de 2019. Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/salmonella-%28non-typhoidal%29
Rabsch W, Andrews HL, Kingsley RA, Prager R, Tschäpe H, Adams LG, et al. Salmonella enterica serotype Typhimurium and its host-adapted variants. Infect Immun. 2002;70:2249-55. https://doi.org/10.1128/IAI.70.5.2249-2255.2002
Leekitcharoenphon P, Hendriksen RS, Le Hello S, Weill F-X, Baggesen DL, Jun S-R, et al. Global genomic epidemiology of Salmonella enterica serovar Typhimurium DT104. Appl Environ Microbiol. 2016;82:2516-26. https://doi.org/10.1128/AEM.03821-15
Kingsley RA, Msefula CL, Thomson NR, Kariuki S, Holt KE, Gordon MA, et al. Epidemic multiple drug resistant Salmonella Typhimurium causing invasive disease in sub-Saharan Africa have a distinct genotype. Genome Res. 2009;19:2279-87. https://doi.org/10.1101/gr.091017.109
Wang X, Biswas S, Paudyal N, Pan H, Li X, Fang W, et al. Antibiotic resistance in Salmonella Typhimurium isolates recovered from the food chain through national antimicrobial resistance monitoring system between 1996 and 2016. Front Microbiol. 2019;10:985. https://doi.org/10.3389/fmicb.2019.00985
Deng Y, Bao X, Ji L, Chen L, Liu J, Miao J, et al. Resistance integrons: Class 1, 2 and 3 integrons. Ann Clin Microbiol Antimicrob. 2015;14:45. https://doi.org/10.1186/s12941-015-0100-6
Partridge SR, Kwong SM, Firth N, Jensen SO. Mobile genetic elements associated with antimicrobial resistance. Clin Microbiol Rev. 2018;31. https://doi.org/10.1128/CMR.00088-17
Okoro CK, Kingsley RA, Connor TR, Harris SR, Parry CM, Al-Mashhadani MN, et al. Intracontinental spread of human invasive Salmonella Typhimurium pathovariants in sub-Saharan Africa. Nat Genet. 2012;44:1215-21. https://doi.org/10.1038/ng.2423
Monte DFM, Sellera FP, Lopes R, Keelara S, Landgraf M, Greene S, et al. Class 1 integronborne cassettes harboring blaCARB-2 gene in multidrug-resistant and virulent Salmonella Typhimurium ST19 strains recovered from clinical human stool samples, United States. PLoS ONE. 2020;15:e0240978. https://doi.org/10.1371/journal.pone.0240978
Maldonado NA, Múnera MI, López JA, Sierra P, Robledo CG, Robledo J, et al. Tendencias de la resistencia a antibióticos en Medellín y municipios del Área Metropolitana entre 2007-2012: resultados de seis años de vigilancia. Biomédica. 2014;34:433-46. https://doi.org/10.7705/biomedica.v34i3.1658
Instituto Nacional de Salud. Informe de Vigilancia por Laboratorio de Salmonella spp.: “Colombia 1997-2018.” Bogotá: Instituto Nacional de Salud; 2019. p. 25.
Ministerio de Salud y Protección Social. Plan Nacional de Respuesta a la resistencia a los antimicrobianos. Plan estratégico. Bogotá: Minsalud; 2018.
Arksey H, O’Malley L. Scoping studies: Towards a methodological framework. Int J Soc Res Methodol. 2005;8:19-32. https://doi.org/10.1080/1364557032000119616
Peters MDJ, Godfrey CM, Khalil H, McInerney P, Parker D, Soares CB. Guidance for conducting systematic scoping reviews. Int J Evid Based Healthc. 2015;13:141-6. https://doi.org/10.1097/XEB.0000000000000050
National Center for Emerging and Zoonotic Infectious Diseases (NCEZID), Division of Foodborne, Waterborne, and Environmental Diseases (DFWED). Glossary of Terms Related to Antibiotic Resistance | NARMS | CDC [Internet]. National Antimicrobial Resistance Monitoring System for Enteric Bacteria (NARMS). 2019. Fecha de consulta: 29 de octubre de 2023. Disponible en: https://www.cdc.gov/narms/resources/glossary.html
Rodríguez EC, Díaz-Guevara P, Moreno J, Bautista A, Montaño L, Realpe ME, et al. Laboratory surveillance of Salmonella enterica from human clinical cases in Colombia 2005-2011. Enferm Infecc Microbiol Clin. 2017;35:417-25. https://doi.org/10.1016/j.eimc.2016.02.023
Moher D, Liberati A, Tetzlaff J, Altman DG, PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: The PRISMA statement. PLoS Med. 2009;6:e1000097. https://doi.org/10.1371/journal.pmed.1000097
Akinyemi KO, Ajoseh SO. Factors contributing to the emergence and spread of antibiotics resistance in salmonella species. In: Mares M, editor. Current topics in salmonella and salmonellosis. InTech; 2017. https://doi.org/10.5772/67701
Dessie HK, Bae DH, Lee YJ. Characterization of integrons and their cassettes in Escherichia coli and Salmonella isolates from poultry in Korea. Poult Sci. 2013;92:3036-43. https://doi.org/10.3382/ps.2013-03312
Roberts MC, Schwarz S. Tetracycline and phenicol resistance genes and mechanisms: Importance for agriculture, the environment, and humans. J Environ Qual. 2016;45:576-92. https://doi.org/10.2134/jeq2015.04.0207
Roberts MC. Tetracycline resistance determinants: Mechanisms of action, regulation of expression, genetic mobility, and distribution. FEMS Microbiol Rev. 1996;19:1-24. https://doi.org/10.1111/j.1574-6976.1996.tb00251.x
White PA, McIver CJ, Rawlinson WD. Integrons and gene cassettes in the enterobacteriaceae. Antimicrob Agents Chemother. 2001;45:2658-61. https://doi.org/10.1128/AAC.45.9.2658-2661.2001
Leverstein-van Hall MA, Blok HEM, Donders RT, Paauw A, Fluit AC, Verhoef J. Multidrug resistance among Enterobacteriaceae is strongly associated with the presence of integrons and is independent of species or isolate origin. J Infect Dis. 2003;187:251-9. https://doi.org/10.1086/345880
Jia C, Wang Z, Huang C, Teng L, Zhou H, An H, et al. Mobilome-driven partitions of the resistome in Salmonella. mSystems. 2023;e0088323. https://doi.org/10.1128/msystems.00883-23
European Food Safety Authority, European Centre for Disease Prevention and Control. The European Union One Health 2019 zoonoses report. EFSA J. 2021;19:e06406. https://doi.org/10.2903/j.efsa.2021.6406
Simpson KMJ, Hill-Cawthorne GA, Ward MP, Mor SM. Diversity of Salmonella serotypes from humans, food, domestic animals and wildlife in New South Wales, Australia. BMC Infect Dis. 2018;18:623. https://doi.org/10.1186/s12879-018-3563-1
Lammie SL, Hughes JM. Antimicrobial resistance, food safety, and one health: The need for convergence. Annu Rev Food Sci Technol. 2016;7:287-312. https://doi.org/10.1146/annurev-food-041715-033251
World Health Organization. Global antimicrobial resistance surveillance system (GLASS) report: Early implementation 2017-2018. Geneva: World Health Organization; 2018. p. 164.
Anderson ES. Drug resistance in Salmonella Typhimurium and its implications. BMJ. 1968;3:333-9. https://doi.org/10.1136/bmj.3.5614.333
Huyan J, Tian Z, Zhang Y, Zhang H, Shi Y, Gillings MR, et al. Dynamics of class 1 integrons in aerobic biofilm reactors spiked with antibiotics. Environ Int. 2020;140:105816. https://doi.org/10.1016/j.envint.2020.105816
World Health Organization. Critically important antimicrobials for human medicine. 5th rev. Geneva: World Health Organization; 2017.
World Health Organization. Critically important antimicrobials for human medicine. 6th revision. Geneva: World Health Organization; 2019.
Guerra B, Soto S, Cal S, Mendoza MC. Antimicrobial resistance and spread of class 1 integrons among Salmonella serotypes. Antimicrob Agents Chemother. 2000;44:2166-9. https://doi.org/10.1128/AAC.44.8.2166-2169.2000
Madec JY, Doublet B, Ponsin C, Cloeckaert A, Haenni M. Extended-spectrum β-lactamase blaCTX-M-1 gene carried on an IncI1 plasmid in multidrug-resistant Salmonella enterica serovar Typhimurium DT104 in cattle in France. J Antimicrob Chemother. 2011;66:942-4. https://doi.org/10.1093/jac/dkr014
Gallardo F, Ruiz J, Soto SM, Jiménez de Anta MT, Vila J. Distintos mecanismos de resistencia asociados a integrones en aislamientos clínicos de Salmonella Typhimurium. Rev Esp Quimioter. 2003;16:398-402.
Partridge SR, Tsafnat G, Coiera E, Iredell JR. Gene cassettes and cassette arrays in mobile resistance integrons. FEMS Microbiol Rev. 2009;33:757-84. https://doi.org/10.1111/j.1574-6976.2009.00175.x
Pulecio-Santos S, Bermúdez-Duarte P, Suárez Alfonso MC. Susceptibilidad antimicrobiana de aislamientos de Salmonella enterica obtenidos del pre-beneficio y de porcinos en Colombia. Rev Salud Pública. 2015;17:106-19. https://doi.org/10.15446/rsap.v17n1.45716
O’Mahony R, Quinn T, Drudy D, Walsh C, Whyte P, Mattar S, et al. Antimicrobial resistance in nontyphoidal Salmonella from food sources in Colombia: Evidence for an unusual plasmid-localized class 1 integron in serotypes Typhimurium and Anatum. Microb Drug Resist. 2006;12:269-77. https://doi.org/10.1089/mdr.2006.12.269
Flórez-Delgado NY, Ubillus EN, Pérez-Sepúlveda B, Ospina-Ríos EL, Carrascal-Camacho AK, Chamorro-Tobar IC, et al. Class 1 integrons in clinical and swine industry isolates of Salmonella Typhimurium from Colombia, dating 1997 to 2017. J Med Microbiol. 2023;72. https://doi.org/10.1099/jmm.0.001704
Balsalobre LC, Dropa M, Matté MH. An overview of antimicrobial resistance and its public health significance. Braz J Microbiol. 2014;45:1-5. https://doi.org/10.1590/S1517-83822014005000033
Organización Mundial de la Salud. Lista OMS de antimicrobianos de importancia crítica para la medicina humana (lista OMS de AIC). Geneva: OMS; 2019. p. 2.
Algunos artículos similares:
- Luz Elena Velásquez, Catalina Gómez, Erika Valencia, Laura Salazar, Eudoro Casas, Estudio de foco de paragonimosis en Fuente Clara, Robledo, área periurbana de Medellín, Antioquia , Biomédica: Vol. 28 Núm. 3 (2008)
- Sandra Milena Arias, Lina Marcela Salazar, Eudoro Casas, Alexandra Henao, Luz Elena Velásquez, Paragonimus sp. en cangrejos y sensibilización de la comunidad educativa hacia los ecosistemas acuáticos de La Miel y La Clara, Caldas, Antioquia , Biomédica: Vol. 31 Núm. 2 (2011)
- Jaiberth Cardona-Arias, Luz Peláez-Vanegas, Juan López-Saldarriaga, Marcela Duque-Molina, Oscar Leal-Álvarez, Calidad de vida relacionada con la salud en adultos con VIH/sida, Medellín, Colombia, 2009 , Biomédica: Vol. 31 Núm. 4 (2011)
- Jacqueline Chaparro, Moisés Wasserrnanz, Adecuación de una prueba radiométrica para la detección de resistencia múltiple de Plasmodium falciparum a medicamentos , Biomédica: Vol. 19 Núm. 1 (1999)
- Jacqueline Chaparro, Moisés Wasserman, Comparación de técnicas in vitro para detectar resistencia de Plasmodium falciparum a medicamentos , Biomédica: Vol. 19 Núm. 2 (1999)
- Eliana P. Calvo, María O. Rojas, Jacqueline Chaparro, Moisés Wasserman, Expresión del gen asociado con la resistencia múltiple a medicamentos (pfmdrl) en cepas colombianas de Plasmodium falciparum , Biomédica: Vol. 19 Núm. 3 (1999)
- Oscar G. Gómez, Vacuna atenuada de Salmonella como vector de antígenos heterólogos , Biomédica: Vol. 20 Núm. 2 (2000)
- Nélida Muñoz, Clara Inés Agudelo, Maria Victoria Ovalle, María Helena Realpe, Edilma Jaramillo, Sandra Núñez, Martha Uzeta, Vianney Portilla, María del Pilar Crespo, María Elena Alvarez, Constanza Sabogal, Mercedes Cano, María Claudia Rodríguez, María Eugenia Peláez, Lesli Bruzón, Mileny Arregocés, Gloria Patricia Londoño, Gloria Inés Dussán, Liliana Patiño, Alix Robinson, Vigilancia en red de los serotipos y la susceptibilidad antimicrobiana de Salmonella spp., Shigella spp. Y Vibrio cholerae O1, 1997 - 1999 , Biomédica: Vol. 20 Núm. 3 (2000)
- Johnny Durango, Germán Arrieta, Salim Mattar, Presencia de Salmonella spp. en un área del Caribe colombiano: un riesgo para la salud pública. , Biomédica: Vol. 24 Núm. 1 (2004)
- Pamela Orjuela, Iveth González, Lyda Osorio, Terapia combinada como estrategia en la prevención de la resistencia a los antimaláricos. , Biomédica: Vol. 24 Núm. 4 (2004)
Derechos de autor 2024 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























