Diez años del “Programa de evaluación de desempeño de laboratorios de inmunogenética” y su impacto en la “Red de donación y trasplantes”
Resumen
Introducción. El uso de las pruebas inmunológicas antes del trasplante de órganos sólidos es fundamental para disminuir el riesgo de rechazo y las complicaciones de los trasplantes. Los sistemas de control de calidad de los laboratorios que las realizan son, por tanto, necesarios para la práctica clínica. El Instituto Nacional de Salud implementó el “Programa de evaluación externa del desempeño para laboratorios de inmunogenética de trasplantes” en el 2014.
Objetivo. Evaluar el desempeño de los laboratorios con base en los resultados de cinco pruebas inmunológicas para trasplantes en Colombia entre el 2014 y el 2023, según las directrices del “Programa de evaluación externa del desempeño para laboratorios de inmunogenética de trasplantes”.
Materiales y métodos. Se estudió el desempeño de los laboratorios mediante la evaluación de cinco pruebas inmunológicas para trasplante: clasificación del HLA de clase I y II, prueba cualitativa y prueba cuantitativa para el panel de anticuerpos reactivos, PRA (Panel Reactive Antibodies), pruebas para antígenos individuales y pruebas cruzadas. Se recolectaron los datos de los informes de cada laboratorio. Con base en las comparaciones entre laboratorios, se calificó el desempeño de cada uno como «bueno», «aceptable» o «inaceptable» para cada prueba. Se calcularon proporciones y se hizo un análisis de valores predichos con intervalos de confianza del 95 %.
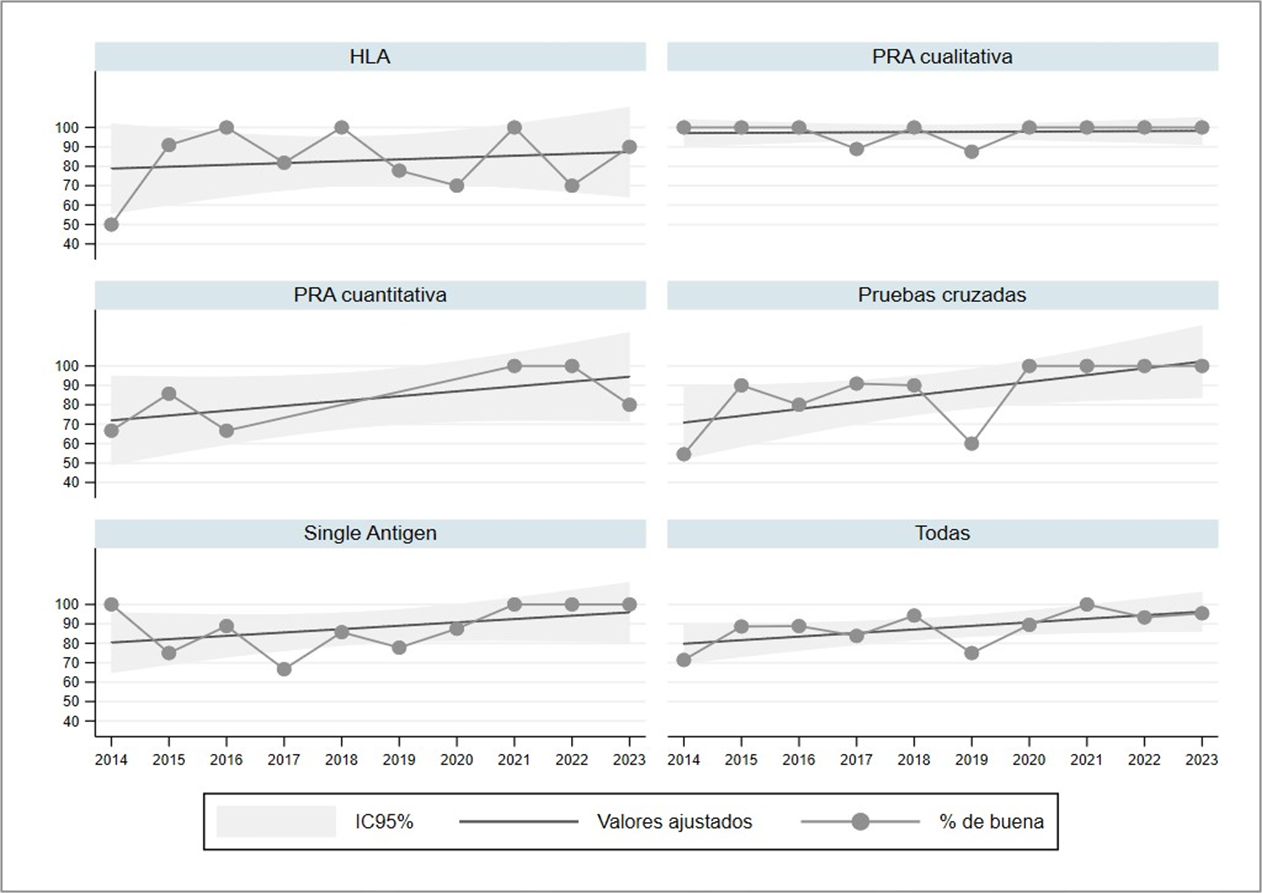
Resultados. El número de laboratorios participantes varió entre 5 y 12 para cada prueba. La categoría de desempeño «buena» fue menor en el primer año. El mejor resultado fue para la PRA cualitativa, calificada como «buena» en todos los laboratorios durante ocho años. En las pruebas de HLA (2014), PRA cualitativo (2017 y 2019), pruebas cruzadas (2019) y single antigen (2017 y 2019), el porcentaje de laboratorios con desempeño catalogado como «bueno» fue menor que el esperado.
Conclusión. El desempeño observado fue «bueno» en todos los laboratorios en el último trienio, excepto para dos de las cinco pruebas: el HLA y la PRA (Panel Reactive Antibodies) cuantitativa.
Descargas
Referencias bibliográficas
Prieto L, Salinas MA, Arias YR, Rodríguez LM, Giraldo MC, Suárez DM, et al. Estándares de calidad para laboratorios que realizan pruebas de inmunogenética para trasplante de órganos. 2013. Fecha de consulta: 24 de febrero de 2024. Disponible en: https://www.ins.gov.co/Direcciones/RedesSaludPublica/GestiondeCalidadLaboratorios/ConsultaEstandaresparaLaboratoriosdeInmunologia/Estandares%20para%20laboratorios%20de%20inmunologia%20version%20online%202013.pdf
The American Society for Histocompatibility and Immunogenetics. Quality assurance and standards. Fecha de consulta: 24 de febrero de 2024. Disponible en: https://www.ashi-hla.org/page/standards
European Federation for Immunogenetics. Standards for histocompatibility immunogenetics. Fecha de consulta: 24 de febrero de 2024. Disponible en: https://efi-web.org/fileadmin/Efi_web/Standardv8_280819.pdf
McHugh ML. Interrater reliability: The kappa statistic. Biochem Med (Zagreb). 2012;22:276-82.
Ministerio de Salud. Resolución 8430 del 4 de octubre de 1993. Fecha de consulta: 30 de mayo de 2024. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/DE/DIJ/RESOLUCION-8430-DE-1993.pdf
Zhao X, Ma S, Wang B, Jiang X, The Han100K Initiative, Xu S. PGG.MHC: Toward understanding the diversity of major histocompatibility complexes in human populations. Nucleic Acids Res. 2023;51:D1102-8. https://doi.org/10.1093/nar/gkac997
Apps R, Qi Y, Carlson JM, Chen H, Gao X, Thomas R, et al. Influence of HLA-C expression level on HIV control. Science. 2013;340:87-91. https://doi.org/10.1126/science.1232685
Díaz-Peña R, Castro-Santos P, Aransay AM, Brüges-Armas J, Pimentel-Santos FM, López-Larrea C. Genetic study confirms association of HLA-DPA1*01:03 subtype with ankylosing spondylitis in HLA-B27-positive populations. Hum Immunol. 2013;74:764-7. https://doi.org/10.1016/j.humimm.2013.02.001
Migliorini F, Torsiello E, Spiezia F, Oliva F, Tingart M, Maffulli N. Association between HLA genotypes and COVID-19 susceptibility, severity and progression: A comprehensive review of the literature. Eur J Med Res. 2021;26:84. https://doi.org/10.1186/s40001-021-00563-1
Zeestraten ECM, Reimers MS, Saadatmand S, Goossens-Beumer IJ, Dekker JWT, Liefers GJ, et al. Combined analysis of HLA class I, HLA-E and HLA-G predicts prognosis in colon cancer patients. Br J Cancer. 2014;110:459-68. https://doi.org/10.1038/bjc.2013.696.
Montgomery RA, Tatapudi VS, Leffell MS, Zachary AA. HLA in transplantation. Nat Rev Nephrol. 2018;14:558-70. https://doi.org/10.1038/s41581-018-0039-x
Arias-Murillo YR, Salinas-Nova Ma, Montaño Ji. Criterios de asignación para trasplante renal en Colombia. Fecha de consulta: 12 de junio de 2024. Disponible en: https://www.ins.gov.co/BibliotecaDigital/consenso-criterios-asignacion-trasplante-renal-colombia.pdf
Salinas-Nova MA, Arias-Murillo YR, Patiño-Amaya YA, Rivera T, Jiménez-Urrea V, Pineda-Lozano JC, et al. Conferencia de consenso de recomendaciones para la construcción de un documento nacional de criterios de asignación para trasplante de corazón en Colombia. Instituto Nacional de Salud; 2022. Fecha de consulta: 12 de junio de 2024. Disponible en: https://www.ins.gov.co/BibliotecaDigital/consenso-criterios-de-asignacion-para-trasplantecardiaco-en-colombia.pdf
Instituto Nacional de Salud. Conferencia de consenso de criterios de asignación para trasplante de pulmón en Colombia. 2022. Fecha de consulta: 12 de junio de 2024. Disponible en: https://www.ins.gov.co/BibliotecaDigital/resultados-consenso-de-pulmon.pdf
Instituto Nacional de Salud. Informe ejecutivo Red de Donación y Trasplantes 2023. Fecha de consulta: 12 de junio de 2024. Disponible en: https://www.ins.gov.co/BibliotecaDigital/informe-ejecutivo-colombia-2023-anual.pdf
Instituto Nacional de Salud. Inscripción a los programas de evaluación externa del desempeño (PEED). Fecha de consulta: 12 de junio de 2024. Disponible en: https://www.ins.gov.co/TyS/programas-de-calidad
Levering WH, van den Beemd R, Marvelde JG, van Beers WA, Hooijkaas H, Sintnicolaas K, et al. External quality assessment of flow cytometric HLA-B27 typing. Cytometry. 2000;42:95-105.
Macardle PJ, McEvoy R, Jovanovich S. HLA-B27 expression by flow cytometry: An analysis of seven years quality assurance data. J Immunol Methods. 2000;243:51-7. https://doi.org/10.1016/s0022-1759(00)00227-1
Voorter CEM, Groeneveld L, Heidt S, Wieten L. Evaluation of 19 years of international external proficiency testing for high-resolution HLA typing. Front Genet. 2024;14:1290915. https://doi.org/10.3389/fgene.2023.1290915
Harmer A, Mascaretti L, Petershofen E. Accreditation of histocompatibility and immunogenetics laboratories: Achievements and future prospects from the European Federation for Immunogenetics Accreditation Programme. HLA. 2018;92:67-73. https://doi.org/10.1111/tan.13289
Lin G, Zhang K, Li J. A national proficiency scheme for human leucocyte antigen typing by next-generation sequencing. Clin Chim Acta. 2022;533:85-8. https://doi.org/10.1016/j.cca.2022.06.015
Duquesnoy RJ, Marrari M. Multilaboratory evaluation of serum analysis for HLA antibody and crossmatch reactivity by lymphocytotoxicity methods. Arch Pathol Lab Med. 2003;127:149-56. https://doi.org/10.5858/2003-127-149-MEOSAF
Chong AS. Mechanisms of organ transplant injury mediated by B cells and antibodies: Implications for antibody-mediated rejection. Am J Transplant. 2020;20:23-32. https://doi.org/10.1111/ajt.15844
Loupy A, Hill GS, Jordan SC. The impact of donor-specific anti-HLA antibodies on late kidney allograft failure. Nat Rev Nephrol. 2012;8:348-57. https://doi.org/10.1038/nrneph.2012.81
Tait BD, Süsal C, Gebel HM, Nickerson PW, Zachary AA, Claas FHJ, et al. Consensus guidelines on the testing and clinical management issues associated with HLA and non-HLA antibodies in transplantation. Transplantation. 2013;95:19-47. https://doi.org/10.1097/TP.0b013e31827a19cc
Reinsmoen NL, Lai CH, Vo A, Cao K, Ong G, Naim M, et al. Acceptable donor-specific antibody levels allowing for successful deceased and living donor kidney transplantation after desensitization therapy. Transplantation. 2008;86:820-5. https://doi.org/10.1097/TP.0b013e3181856f98
Cecka JM. Current methodologies for detecting sensitization to HLA antigens. Curr Opin Organ Transplant. 2011;16:398-403. https://doi.org/10.1097/MOT.0b013e328348980a
Rodríguez-Ramírez S. Al Jurdi AD. Konvalinka AG. Riella L. Antibody-mediated rejection: Prevention, monitoring and treatment dilemmas. Curr Opin Organ Transplant. 2022;27:405-14. https://doi.org/10.1097/MOT.0000000000001011
Tait BD, Hudson F, Brewin G, Cantwell L, Holdsworth R. Solid phase HLA antibody detection technology--challenges in interpretation. Tissue Antigens. 2010;76:87-95. https://doi.org/10.1111/j.1399-0039.2010.01486.x
Oh EJ, Park H, Park KU, Kang ES, Kim HS, Song EY. Interlaboratory comparison of the results of lifecodes LSA class I and class II single antigen kits for human leukocyte antigen antibody detection. Ann Lab Med. 2015;35:321-8. https://doi.org/10.3343/alm.2015.35.3.321
Algunos artículos similares:
- Paula Ximena Pavía, Nubia Lucía Roa, Ana María Uribe, Concepción Judith Puerta, Seguimiento de paciente con enfermedad de Chagas y trasplante de corazón mediante las PCR S35-S36 y TcH2AF-R , Biomédica: Vol. 31 Núm. 2 (2011)
- John F. Arboleda, Luis F. García, Cristiam M. Álvarez, Papel de las células dendríticas tolerogénicas ILT3+/ILT4+ en la respuesta inmunitaria a trasplante de órganos y tejidos , Biomédica: Vol. 31 Núm. 2 (2011)
- Lorenzo Cáceres, José Rovira, Rolando Torres, Arsenio García, José Calzada, Manuel De La Cruz, Caracterización de la transmisión de la malaria por Plasmodium vivax en la región fronteriza de Panamá con Costa Rica en el municipio de Barú, Panamá , Biomédica: Vol. 32 Núm. 4 (2012)
- Carmen E. Alarcón, Hernán Hurtado, Jaime E. Castellanos, Anticuerpos aviares: alternativa en producción y diagnóstico , Biomédica: Vol. 20 Núm. 4 (2000)
- Mario García, Liliana Alejandra Chicaíza, Hoover Quitián, Adriana Linares, Óscar Ramírez, Costo-efectividad de los tratamientos de consolidación para la leucemia mieloide aguda en niños en riesgo alto en el sistema de salud colombiano , Biomédica: Vol. 35 Núm. 4 (2015)
- Yazmin Rocío Arias, Karime Osorio-Arango, Brayan Bayona, Guadalupe Ercilla, Mauricio Beltrán-Durán, Determinación del polimorfismo HLA -A, -B, -DRB1 en donantes de órganos en muerte encefálica representativos de la población general colombiana, 2007-2014 , Biomédica: Vol. 37 Núm. 2 (2017)
- Lina Echeverri-Toro, Andrés Arango, Sigifredo Ospina, Carlos Agudelo, Bacteriemia recurrente por Bordetella bronchiseptica en un paciente con trasplante de medula ósea , Biomédica: Vol. 35 Núm. 3 (2015)
- Fiona Xacur-García, Rodrigo Díaz-Novelo, Linnete Herrera-David, Paulina Moreno-Arjona, Nina Méndez-Domínguez, Manifestaciones clínicas y evolución a largo plazo de tres casos de rosácea ocular atendidos en un hospital de alta especialidad del sureste de México , Biomédica: Vol. 40 Núm. 3 (2020)
- Julio Cesar Padilla-Rodríguez , Mario Javier Olivera, Pablo Chaparro , Martha Lucía Quiñonez , José Pablo Escobar , Gilberto Álvarez , La campaña de erradicación de la malaria en Colombia, 1959-1979 , Biomédica: Vol. 42 Núm. 2 (2022)
- Andrés Felipe Zea-Vera, Lina María Castaño-Jaramillo, Navegando la transición: desafíos y oportunidades en la atención de los pacientes con errores innatos de la inmunidad , Biomédica: Vol. 44 Núm. Sp. 2 (2024): Inmunología clínica
Derechos de autor 2024 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























