Análisis comparativo de la actividad antimicrobiana de secreciones y excreciones larvales de Calliphora vicina y Sarconesiopsis magellanica (Diptera: Calliphoridae)
Resumen
Introducción. La creciente resistencia bacteriana a los antibióticos representa una amenaza mundial de salud pública. Las excreciones y secreciones larvarias derivadas de moscas necrófagas de la familia Calliphoridae podrían configurar una fuente promisoria para contrarrestar sus efectos.
Objetivo. Comparar la actividad antimicrobiana de las excreciones y secreciones larvarias nativas, y de las mayores y menores de 10 kDa de Calliphora vicina y Sarconesiopsis magellanica (Diptera: Calliphoridae).
Materiales y métodos. El bioensayo se hizo a partir de la técnica de turbidimetría y en el caso de las excreciones y secreciones menores de 10 kDa se determinó la concentración inhibitoria mínima (CIM).
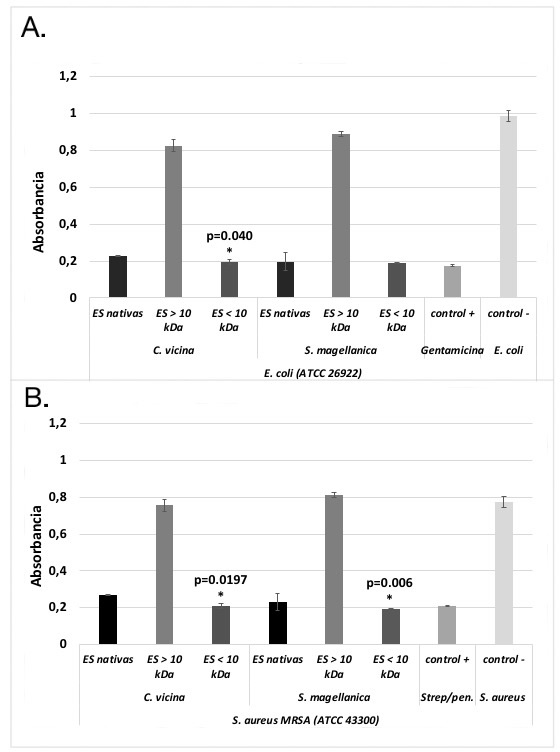
Resultados. Las excreciones y secreciones nativas y las menores de 10 kDa de C. vicina y S. magellanica, evidenciaron una potente actividad antibacteriana contra tres cepas de Staphylococcus aureus y cuatro bacterias Gram negativas, siendo las menores de 10 kDa más efectivas que las nativas en las dos especies de moscas evaluadas. Además, las menores de 10 kDa presentaron la misma efectividad, aunque en las pruebas de CIM se observó que las de S. magellanica fueron más potentes en todas las bacterias evaluadas, excepto contra la cepa de S. aureus ATCC 25923. Las mayores de 10 kDa no inhibieron el crecimiento bacteriano.
Conclusión. Los resultados validaron, en general, que estas sustancias son fuente importante para el aislamiento y la caracterización de agentes antimicrobianos.
Descargas
Referencias bibliográficas
Pape T, Wolff M, Amat EC. Los califóridos, éstridos, rinofóridos y sarcofágidos (Diptera: Calliphoridae, Oestridae, Rhinophoridae, Sarcophagidae) de Colombia. Biota Colombiana. 2004;39:201-8. https://doi.org/10.21068/BC.V5I2.145
Camacho G. Sucesión de la entomofauna cadavérica y ciclo vital de Calliphora vicina (Diptera: Calliphoridae) como primera especie colonizadora, utilizando cerdo blanco. Revista Colombiana de Entomología. 2005;31:35-9.
Francesconia F, Lupi O. Myiasis. Clin Microbiol Rev. 2012;25:79-105. https://doi.org/10.1128/CMR.00010-11
Getachew S, Gebre-Michael T, Erko B, Balkew M, Medhin G. Non-biting cyclorrhaphan flies (Diptera) as carriers of intestinal human parasites in slum areas of Addis Ababa, Ethiopia. Acta Trop. 2007;103:186-94. https://doi.org/10.1016/j.actatropica.2007.06.005
Sharma R, Kumar Garg R, Gaur JR. Various methods for the estimation of the post mortem interval from Calliphoridae: A review. Egypt J Forensic Sci. 2015;5:1-12. https://doi.org/10.1016/j.ejfs.2013.04.002
Sherman RA. Maggot therapy takes us back to the future of wound care: New and improved maggot therapy for the 21st. century. J Diabetes Sci Technol. 2009;3:336-44. https://doi.org/10.1177/193229680900300215
Sherman RA. Mechanisms of maggot-induced wound healing: What do we know, and where do we go from here? Evidence-Based Complement Altern Med. 2014:2014:1-13. https://doi.org/10.1155/2014/592419
Choudhary V, Choudhary M, Pandey S, Chauhan VD, Hasnani JJ. Maggot debridement therapy as primary tool to treat chronic wound of animals. Vet World. 2016;9:403-9. https://doi.org/10.14202/vetworld.2016.403-409
van der Plas MJA, Jukema GN, Wai SW, Dogterom-Ballering HCM, Lagendijk EI, van Gulpen C, et al. Maggot excretions/secretions are differentially effective against biofilms of Staphylococcus aureus and Pseudomonas aeruginosa. J Antimicrob Chemother. 2008;61:117-22. https://doi.org/10.1093/jac/dkm407
Mumcuoglu KY, Miller J, Mumcuoglu M, Friger M, Tarshis M. Destruction of bacteria in the digestive tract of the maggot of Lucilia sericata (Diptera: Calliphoridae). J Med Entomol. 2009;38:161-6. https://doi.org/10.1603/0022-2585-38.2.161
Parnés A, Lagan KM. Larval therapy in wound management: A review. Int J Clin Pract. 2007;61:488-93. https://doi.org/10.1111/j.1742-1241.2006.01238.x
Jansen KU, Knirsch C, Anderson AS. The role of vaccines in preventing bacterial antimicrobial resistance. Nat Med. 2018;24:10-20. https://doi.org/10.1038/nm.4465
Bexfield A, Nigam Y, Thomas S, Ratcliffe NA. Detection and partial characterisation of two antibacterial factors from the excretions/secretions of the medicinal maggot Lucilia sericata and their activity against methicillin-resistant Staphylococcus aureus (MRSA). Microbes Infect. 2004;6:1297-304. https://doi.org/10.1016/j.micinf.2004.08.011
Hassan MI, Amer MS, Hammad KM, Zidan MM. Antimicrobial activity for excretion and secretion. J Egypt Soc Parasitol. 2016;46:179-84. https://doi.org/10.12816/0026163
Díaz-Roa A, Gaona MA, Segura NA, Suárez D, Patarroyo MA, Bello FJ. Sarconesiopsis magellanica (Diptera: Calliphoridae) excretions and secretions have potent antibacterial activity. Acta Trop. 2014;136:37-43. https://doi.org/10.1016/j.actatropica.2014.04.018
Barnes KM, Gennard DE, Dixon RA. An assessment of the antibacterial activity in larval excretion/secretion of four species of insects recorded in association with corpses, using Lucilia sericata Meigen as the marker species. Bull Entomol Res. 2010;100:635-40. https://doi.org/10.1017/S000748530999071X
Ratcliffe NA, Vieira CS, Mendonça PM, Caetano RL, Queiroz MM de C, Garcia ES, et al. Detection and preliminary physico-chemical properties of antimicrobial components in the native excretions/secretions of three species of Chrysomya (Diptera: Calliphoridae) in Brazil. Acta Trop. 2015;147:6-11. https://doi.org/10.1016/j.actatropica.2015.03.021
Fonseca-Muñoz A, Pérez-Pacheco R, Ortega-Morales BO, Reyes-Estebanez M, Vásquez-López A, Chan-Bacab M, et al. Bactericidal activity of Chrysomya rufifacies and Cochliomyia macellaria (Diptera: Calliphoridae) larval excretions-secretions against Staphylococcus aureus (Bacillales: Staphylococcaceae). J Med Entomol. 2019;56:1598-604. https://doi.org/10.1093/jme/tjz109
Amat E, Vélez MC, Wolff M. Illustrated key for identification to genera and species of blowflies (Diptera: Calliphoridae) of Colombia. Caldasia. 2008;30:231-44.
Mitchell AM, Mitchell TJ. Streptococcus pneumoniae: Virulence factors and variation. Clin Microbiol Infect. 2010;16:411-8. https://doi.org/10.1111/j.1469-0691.2010.03183.x
Bexfield A, Bond AE, Roberts EC, Dudley E, Nigam Y, Thomas S, et al. The antibacterial activity against MRSA strains and other bacteria of a <500 Da fraction from maggot excretions/secretions of Lucilia sericata (Diptera: Calliphoridae). Microbes Infect. 2008;10:325-33. https://doi.org/10.1016/j.micinf.2007.12.011
Čeřovský V, Žďárek J, Fučík V, Monincová L, Voburka Z, Bém R. Lucifensin, the long-sought antimicrobial factor of medicinal maggots of the blowfly Lucilia sericata. Cell Mol Life Sci. 2010;67:455-66. https://doi.org/10.1007/s00018-009-0194-0
Kawabata T, Mitsui H, Yokota K, Ishino K, Oguma K, Sano S. Induction of antibacterial activity in larvae of the blowfly Lucilia sericata by an infected environment. Med Vet Entomol. 2010;24:375-81. https://doi.org/10.1111/j.1365-2915.2010.00902.x
Van der Plas MJA, Dambrot C, Dogterom-Ballering HCM, Kruithof S, van Dissel JT, Nibbering PH. Combinations of maggot excretions/secretions and antibiotics are effective against Staphylococcus aureus biofilms and the bacteria derived therefrom. J Antimicrob Chemother. 2010;65:917-23. https://doi.org/10.1093/jac/dkq042
Cazander G, Pawiroredjo JS, Vandenbroucke-Grauls CMJE, Schreurs MWJ, Jukema GN. Synergism between maggot excretions and antibiotics. Wound Repair Regen. 2010;18:637-42. https://doi.org/10.1111/j.1524-475X.2010.00625.x
Esparza G. Bacterias Gram negativas resistentes a carbapenémicos en Colombia: un desafío continuo al sistema de salud. Infectio. 2020;24:55-6. https://doi.org/10.22354/in.v24i2.831
Arora S, Baptista C, Lim CS. Maggot metabolites and their combinatory effects with antibiotic on Staphylococcus aureus. Ann Clin Microbiol Antimicrob. 2011;10:6. https://doi.org/10.1186/1476-0711-10-6
Hirsch R, Wiesner J, Marker A, Pfeifer Y, Bauer A, Hammann PE, et al. Profiling antimicrobial peptides from the medical maggot Lucilia sericata as potential antibiotics for MDR Gramnegative bacteria. J Antimicrob Chemother. 2019;74:96-107. https://doi.org/10.1093/jac/dky386
Díaz-Roa A, Espinoza-Culupú A, Torres-García O, Borges MM, Avino IN, Alves FL, et al. Sarconesin II, a new antimicrobial peptide isolated from Sarconesiopsis magellanica excretions and secretions. Molecules. 2019;24:1-27. https://doi.org/10.3390/molecules24112077
Díaz-Roa A, Patarroyo MA, Bello FJ, Da Silva PI. Sarconesin: Sarconesiopsis magellanica blowfly larval excretions and secretions with antibacterial properties. Front Microbiol. 2018;9:1-13. https://doi.org/10.3389/fmicb.2018.02249
Alnaimat SM, Wainwright M, Aladaileh SH. An initial in vitro investigation into the potential therapeutic use of Lucilia sericata maggot to control superficial fungal infections. Jordan J Biol Sci. 2013;6:137-42. https://doi.org/10.12816/0000271
Evans R, Dudley E, Nigam Y. Detection and partial characterization of antifungal bioactivity from the secretions of the medicinal maggot, Lucilia sericata. Wound Repair Regen. 2015;23:361-8. https://doi.org/10.1111/wrr.12287
van der Plas MJA, van der Does AM, Baldry M, Dogterom-Ballering HCM, van Gulpen C, van Dissel JT, et al. Maggot excretions/secretions inhibit multiple neutrophil pro-inflammatory responses. Microbes Infect. 2007;9:507-14. https://doi.org/10.1016/j.micinf.2007.01.008
Pöppel AK, Kahl M, Baumann A, Wiesner J, Gökçen A, Beckert A, et al. A Jonahlike chymotrypsin from the therapeutic maggot Lucilia sericata plays a role in wound debridement and coagulation. Insect Biochem Mol Biol. 2016;70:138-47. http://doi.org/10.1016/j.ibmb.2015.11.012
Kahl M, Gôkçen A, Fischer S, Bäumer M, Wiesner J, Lochnit G, et al. Maggot excretion products from the blowfly Lucilla sericata contain contact phase/intrinsic pathway-like proteases with procoagulant functions. Thromb Haemost. 2015;114:277-88. http://doi.org/10.1160/TH14-06-0499
Algunos artículos similares:
- Virgilio Galvis, Alejandro Tello, Alfredo Guerra, María Fernanda Acuña, Donaldo Villarreal, Sensibilidad antibiótica de bacterias obtenidas de queratitis e infecciones intraoculares en la Fundación Oftalmológica de Santander (FOSCAL), Floridablanca, Colombia , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Andrés Leonardo González, Aura Lucía Leal, Jorge Alberto Cortés, Ricardo Sánchez, Liliana Isabel Barrero, Juan Sebastián Castillo, Carlos Arturo Álvarez, Efecto del tratamiento antibiótico inicial adecuado sobre la mortalidad en pacientes en estado crítico con bacteriemia por Pseudomonas aeruginosa , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Marlen Cháves, Caracterización de reacciones adversas a medicamentos en adultos mayores de 44 años en Bogotá, D.C., enero a diciembre, 2012 , Biomédica: Vol. 35 Núm. 1 (2015)
- Christian José Pallares, Ernesto Martínez, Factores de riesgo asociados a mortalidad en infecciones relacionadas con la atención en salud en un hospital universitario de tercer nivel en Colombia , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Adriana Jiménez, Alejandra Alvarado, Felipe Gómez, Germán Carrero, Claudia Fajardo, Factores de riesgo asociados al aislamiento de Escherichia coli o Klebsiella pneumoniae productoras de betalactamasas de espectro extendido en un hospital de cuarto nivel en Colombia , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Manuel Medell, Marcia Hart, María Luisa Batista, Sensibilidad antimicrobiana in vitro en aislamientos de Enterococcus faecalis y Enterococcus faecium obtenidos de pacientes hospitalizados , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Katerina Klímová, Camilo Padilla, Juan Carlos Ávila, Gerardo Clemente, Alejandra Ochoa, Epidemiología de las infecciones bacterianas en pacientes con cirrosis hepática, experiencia de un centro español de atención terciaria , Biomédica: Vol. 36 Núm. 1 (2016)
- Mónica Alejandra Bernal-Vargas, Jorge Alberto Cortés, Ricardo Sánchez, Adaptación transcultural del cuestionario de puntuación de la neumonía adquirida en la comunidad en pacientes con neumonía leve a moderada en Colombia , Biomédica: Vol. 37 Núm. 1 (2017)
- Carlos Carvajal, Carlos Pacheco, Fabián Jaimes, Perfil clínico y demográfico y factores de riesgo frente a la infección por Clostridium difficile , Biomédica: Vol. 37 Núm. 1 (2017)
- Mónica Tatiana Herrera, Jhon Jhamilton Artunduaga, Claudia Cristina Ortiz, Rodrigo Gonzalo Torres, Síntesis de nanopartículas de ácido poli-láctico cargadas con antibióticos y su actividad antibacteriana contra Escherichia coli O157:H7 y Staphylococcus aureus resistente a meticilina , Biomédica: Vol. 37 Núm. 1 (2017)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























