Caracterización epidemiológica de la infección por Leptospira spp. en caballos de trabajo y en personas ocupacionalmente expuestas en seis unidades de la Policía Nacional de Colombia
Resumen
Introducción. Los caballos de trabajo de la Policía Nacional tienen un estrecho contacto con sus manejadores y la población en general durante las actividades recreativas y de patrullaje, lo cual puede favorecer la transmisión de la leptospirosis en los caballos y el personal ocupacionalmente expuesto.
Objetivo. Caracterizar epidemiológicamente la leptospirosis mediante pruebas de serología, urocultivo y reacción en cadena de la polimerasa (Polymerase Chain Reaction, PCR) en caballos de trabajo y personal con riesgo ocupacional pertenecientes a seis unidades de la Policía Nacional de Colombia.
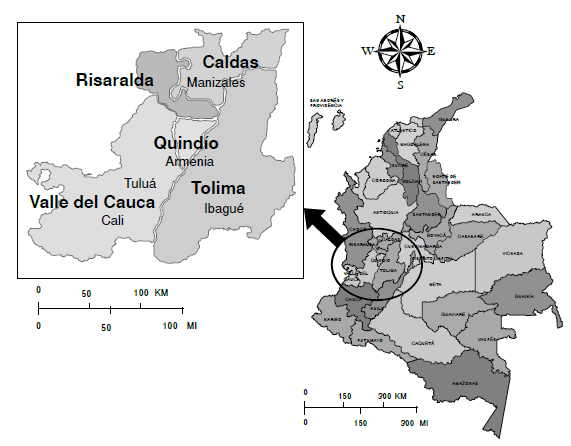
Materiales y métodos. Se evaluaron 153 caballos machos castrados y 123 personas en las seis unidades en los municipios de Manizales, Pereira, Armenia, Ibagué, Tuluá y Cali. Se utilizaron tres formatos estructurados para recabar información y se obtuvieron muestras sanguíneas de las personas y de los caballos, las cuales se procesaron con la prueba de aglutinación microscópica (Macroscopic Agglutination Test, MAT) para 24 serogrupos. Se practicó el examen clínico de los caballos y se obtuvieron muestras de orina para el urocultivo y la PCR convencional.
Resultados. La seroprevalencia de Leptospira spp. fue de 3,25 % (n=4) en las personas y de 85 % (n=130) en los caballos. Entre los caballos, los serogrupos Djasiman y Shermani fueron los más prevalentes. El urocultivo fue positivo en el 64,7 % (99/153) de las muestras, en tanto que los análisis de PCR fueron negativos. Se encontró una asociación estadísticamente significativa de la frecuencia de salida de las instalaciones (p=0,009) y la presencia de fauna silvestre (p=0,051) con la infección por el serogrupo Shermani.
Conclusión. Las características epidemiológicas de la leptospirosis en los caballos sugieren una presentación endémica de la infección y su papel como reservorios de la bacteria; sin embargo, debe dilucidarse la patogenia de la enfermedad con estudios complementarios.
Descargas
Referencias bibliográficas
Levett PN. Leptospirosis: A forgotten zoonosis? Clin Appl Immunol Rev. 2004;4:435-48. https://doi.org/10.1016/j.cair.2004.08.001
Verma A, Stevenson B, Adler B. Leptospirosis in horse. Vet Microbiol. 2013;167:61-6. https://doi.org/10.1016/j.vetmic.2013.04.012.2013
Habus J, Persic Z, Spicic S, Vince S, Zrinka S, Milas Z, et al. New trends in human and animal leptospirosis in Croatia, 2009-2014. Acta Tropica. 2017;168:1-8. https://doi.org/10.1016/j.actatropica.2017.01.002
Tsegay K, Potts AD, Aklilu N, Lötter C, Gummow B. Circulating serovars of Leptospira in cart horses of central and southern Ethiopia and associated risk factors. Prev Vet Med. 2016;125:106-15. https://doi.org/10.1016/j.prevetmed.2016.01.009
Tadich TA, Tapia C, González D. Seroprevalence of Leptospira spp. in working horses located in the Central Region of Chile. J Equine Vet Sci. 2016;38:14-8. https://doi.org/10.1016/j.jevs.2015.12.011
Hamond C, Martins G, Lilenbaum W. Subclinical leptospirosis may impair athletic performance in racing horses. Trop Anim Health Prod. 2012;44:1927-30. https://doi.org/10.1007/s11250-012-0158-5
Mwachui MA, Crump L, Hartskeerl R, Zinsstag J, Hattendorf J. Environmental and behavioural determinants of leptospirosis transmission: A systematic review. PLoS Negl Trop Dis. 2015;9:1-15. https://doi.org/10.1371/journal.pntd.0003843
Hamond C, Martins G, Lawson-Ferreira R, Medeiros MA, Lilenbaum W. The role of horses in the transmission of leptospirosis in an urban tropical area. Epidemiol Infect. 2013;141:33-5. https://doi.org/10.1017/S0950268812000416
Jung BY, Lee KW, Ha TY. Seroprevalence of Leptospira spp. in clinically healthy racing horses in Korea. J Vet Med Sci. 2010;72:197-201. https://doi.org/10.1292/jvms.09-0273
Picardeau M, Bertherat E, Jancloes M, Skouloudis AN, Durski K, Hartskeerl RA. Rapid tests for diagnosis of leptospirosis: Current tools and emerging technologies. Diagn Microbiol Infect Dis. 2014;78:1-8. https://doi.org/10.1016/j.diagmicrobio.2013.09.012
Levett PN, Morey RE, Galloway RL, Turner DE, Steigerwalt AG, Mayer LW. Detection of pathogenic leptospires by real-time quantitative PCR. J Med Microbiol. 2005;54:45-9. https://doi.org/10.1099/jmm.0.45860-0
Kositanont U, Rugsasuk S, Leelaporn A, Phulsuksombati D, Tantitanawat S, Naigowit P. Detection and differentiation between pathogenic and saprophytic Leptospira spp. by multiplex polymerase chain reaction. Diagn Microbiol Infect Dis. 2007;57:117-22. https://doi.org/10.1016/j.diagmicrobio.2006.07.014
Hamond C, Martins G, Lilenbaum W, Madeiros MA. PCR detection of leptospiral carriers among seronegative horses. Vet Rec. 2012;171:105-6. https://doi.org/10.1136/vr.e5022
Levett PN. Leptospirosis. Clin Microbiol. 2001;14:296-326. https://doi.org/10.1128/CMR.14.2.296-326.2001
Agudelo-Flórez P, Restrepo-Jaramillo BN, Arboleda-Naranjo M. Situación de la leptospirosis en el Urabá antioqueño colombiano: estudio seroepidemiológico y factores de riesgo en población general urbana. Cad Saúde Pública. 2007;23:2094-102. https://doi.org/10.1590/S0102-311X2007000900017
Romero MH, Sánchez J, Hayek LC. Prevalencia de anticuerpos contra Leptospira en población urbana humana y canina del departamento del Tolima. Rev Salud Pública. 2010;12:268-75. https://doi.org/10.1590/S0124-00642010000200010
Rey-Riaño LA, Pineda-Rojas NF, Góngora-Orjuela A, Parra-Arango JL, Patiño-Burbano RE. Evaluación serológica a Leptospira spp. en equinos aparentemente sanos en municipios del Meta y Guaviare, Colombia. Revista Lasallista de Investigación 2015;12:154-61.
Troncoso-Toro I, Toro-Barros J, Guzmán-Cáceres A, Fuentealba-Ortega J, Wiethuchter CF. Evaluación serológica de Leptospira interrogans en equinos pertenecientes um centro equestre da província de Linares, Chile. Revista CES de Medicina y Zootecnia 2013;8:101-7.
Scheaffer RL, Mendenhall W, Ott L. Elementos de muestreo. Madrid: Editorial Paraninfo, S.A.; 2006. p. 51
Astudillo-Hernández M, González-Rodríguez A, Batista-Santiesteban N, Mirabal-Sosa M, Menéndez-Hernández J. Estudio seroepidemiológico de la leptospirosis humana en el departamento del Valle del Cauca, Colombia. Revista Cubana de Medicina Tropical 2009;61:1-10.
Organización Mundial de Sanidad Animal (OIE). Manual de las pruebas de diagnóstico y de las vacunas para los animales terrestres (mamíferos, aves y abejas). Quinta edición. Paris: OIE; 2004. p. 1260. http://www.oie.int/doc/ged/d6508.pdf
Moreno N, Flórez PA. Aplicación de las pruebas de PCR convencional simple y múltiple para la identificación de Leptospira spp. en Colombia. Rev Peru Med Exp Salud Pública. 2010;27:548-56.
Langoni H, Da Silva A, Pezerico S, De Lima V. Anti-leptospire agglutinins in equine sera, from São Paulo, Goias, and Mato Grosso do sul, Brazil, 1996-2001. Journal of Venomous Animals and Toxins including Tropical Diseases 2004;10:207-18. https://doi.org/10.1590/S1678-91992004000300003
de Oliveira-Filho RB, Malta KC, Oliveira JM, Assis-Santana VL, Harrop MHV, Stipp DT, et al. Epidemiological analysis of Leptospira spp. infection in equids from the Brejo Paraibano microregion in Brazil. J Equine Vet Sci. 2014;34:407-14. https://doi.org/10.1016/j.jevs.2013.08.001
Finger MA, Barros Filho IR, Leutenegger C, Estrada M, Ullmann LS, Langoni H, et al. Serological and molecular survey of Leptospira spp. among cart horses from an endemic area of human leptospirosis in curitiba, southern Brazil. Rev Inst Med Trop São Paulo. 2014;56:473-6. https://doi.org/10.1590/S0036-46652014000600003
Hashimoto VY, GonÇalves DD, da Silva FG, de Oliveira RC, Alves LA, Reichmann P, et al. Occurrence of antibodies against Leptospira spp. in horses of the urban area of Londrina, Paraná, Brazil. Rev Inst Med Trop São Paulo. 2007;49:327-30. https://doi.org/10.1590/S0036-46652007000500010
Båverud V, Gunnarsson A, Engvall EO, Franzén P, Egenvall A. Leptospira seroprevalence and associations between seropositivity, clinical disease and host factors in horses. Acta Vet Scand. 2009;51:1-10. https://doi.org/10.1186/1751-0147-51-15
Khousheh Y, Hassanpour A, Abdollahpour GR, Mogaddam S. Seroprevalence of leptospira infection in horses in ardabil-iran. Glob Vet. 2012;9:586-9. http://idosi.org/gv/GV9(5)12/14.pdf
Odontsetseg N, Boldbaatar D, Mweene AS, Kida H. Serological prevalence of Leptospira interrogans serovar Bratislava in horses in Mongolia. Vet Rec. 2005;157:518-9. https://doi.org/10.1136/vr.157.17.518
Pikalo J, Sattler T, Eichinger M, Loitsch A, Sun H, Schmoll F, et al. Occurrance of antibodies against Leptospira in horses in Middle Germany. Berl Munch Tierarztl Wochenschr. 2016;129:202-8.
Rocha T, Ellis WA, Montgomery J, Gilmore C, Regalla J, Brem S. Microbiological and serological study of leptospirosis in horses at slaughter: First isolations. Res Vet Sci. 2004;76:199-202. https://doi.org/10.1016/j.rvsc.2003.12.003
Simbizi V, Saulez MN, Potts A, Letter C, Gummow B. A study of leptospirosis in South African horses and associated risk factors. Prev Vet Med. 2016;134:6-15. https://doi.org/10.1016/j.prevetmed.2016.09
Wangdi C, Picard J, Tan R, Condon F, Dowling B, Gummow B. Equine leptospirosis in tropical Northern Queensland. Aust Vet J. 2013;91:190-7. https://doi.org/10.1111/avj.12038
Valencia C, Silva J. Prevalencia de Leptospira spp. en equinos en la sabana de Bogotá (tesis). Bogotá: Universidad de la Salle; 2007.
Bedoya-Ríos MA, Jaimes-Salcedo J, Molina-Sanguino LM. Prevalencia de Leptospira spp. en equinos de la vereda Guatiguara del municipio de Piedecuesta, Santander. Rev Electron Vet. 2013;14:1-6.
Vieira AS, Narduche L, Martins G, Schabib Péres IA, Zimmermann NP, Juliano RS, et al. Detection of wild animals as carriers of Leptospira by PCR in the Pantanal biome, Brazil. Acta Trop. 2016;163:87-9. https://doi.org/10.1016/j.actatropica.2016.08.001
de Albuquerque NF, Martins G, Medeiros L, Lilenbaum W, Ribeiro VM. The role of capybaras as carriers of leptospires in periurban and rural areas in the western Amazon. Acta Trop. 2017;169:57-61. https://doi.org/10.1016/j.actatropica.2017.01.018
Rossetti CA, Liem M, Samartino LE, Hartskeerl RA. Buenos Aires, a new Leptospira serovar of serogroup Djasiman, isolated from an aborted dog fetus in Argentina. Vet Microbiol. 2005;107:241-8. https://doi.org/10.1016/j.vetmic.2005.01.015
Yan W, Faisal SM, Divers T, McDonough SP, Akey B, Chang YF. Experimental Leptospira interrogans serovar Kinnewicki infection of horses. J Vet Intern Med. 2010; 24:912-7. https://doi.org/10.1111/j.1939-1676.2010.0507.x
Hamond C, Pestana CP, Rocha-de-Souza CM, Cunha LE, Brandao FZ, Medeiros MA, et al. Presence of leptospires on genital tract of mares with reproductive problems. Vet Microbiol. 2015;179:264-9. https://doi.org/10.1016/j.vetmic.2015.06.014
Hamond C, Martins G, Bremont S, Medeiros MA, Bourhy P, Lilenbaum W. Molecular characterization and serology of Leptospira kirschneri (Serogroup Grippotyphosa) isolated from urine of a mare post-abortion in Brazil. Zoonoses Public Health. 2016;63:191-5. https://doi.org/10.1111/zph.12224
Calderón A, Rodríguez V, Máttar S, Arrieta G. Leptospirosis in pigs, dogs, rodents, humans, and water in an area of the Colombian tropics. Trop Anim Health Prod. 2014;46:427-32. https://doi.org/10.1007/s11250-013-0508-y
Murray GL, Srikram A, Hoke DE, Wunder EA, Henry R, Lo M, et al. Major surface protein LipL32 is not required for either acute or chronic infection with Leptospira interrogans. Infect Immun. 2009;77:952-8. https://doi.org/10.1128/IAI.01370-08
Algunos artículos similares:
- Lina María Echeverri-Toro, Sara Penagos, Laura Castañeda, Pablo Villa, Santiago Atehortúa, Faiver Ramírez, Carlos Restrepo, Sigifredo Ospina, Yuli Agudelo, Alicia Hidrón, Paola Agudelo, Eliana Valderrama, Carlos Andrés Agudelo, Características sociodemográficas y clínicas de pacientes con infección por Leptospira spp. atendidos en cuatro centros hospitalarios de Medellín, Colombia, 2008-2013 , Biomédica: Vol. 37 Núm. 1 (2017)
- Piedad Agudelo-Flórez, Harold Durango, Diego Aranzazu, Juan David Rodas, Bruno Travi, Genotipificación y evaluación de la dinámica de infección de un aislamiento colombiano de Leptospira santarosai en el modelo experimental en hámster , Biomédica: Vol. 34 Núm. 3 (2014)
- Dionisia Yusti, Margarita Arboleda, Piedad Agudelo-Flórez, Factores de riesgo sociales y ambientales relacionados con casos de leptospirosis de manejo ambulatorio y hospitalario, Turbo, Colombia , Biomédica: Vol. 33 (2013): Suplemento 1, Fiebres hemorrágicas
- Piedad Agudelo Flórez, Marcos Restrepo, María Amparo Lotero, Evaluación de la prueba de inmunofluorescencia indirecta para el diagnóstico de leptospirosis humana. , Biomédica: Vol. 26 Núm. 2 (2006)
- Daniel Eduardo Henao, Fabián Alberto Jaimes, Medicina basada en la evidencia: una aproximación epistemológica , Biomédica: Vol. 29 Núm. 1 (2009)
- Luz Elena Velásquez, Catalina Gómez, Erika Valencia, Laura Salazar, Eudoro Casas, Estudio de foco de paragonimosis en Fuente Clara, Robledo, área periurbana de Medellín, Antioquia , Biomédica: Vol. 28 Núm. 3 (2008)
- Paola Andrea Rueda , Sara Orozco , Juan Raúl Castro , Ángela María Londoño, Elsa María Vásquez, Andrea Arango, Carlos Esteban Builes , Epidemiología del vitiligo: incidencia y prevalencia por sexo y edad en la población colombiana , Biomédica: Vol. 45 Núm. 4 (2025)
- Juan P. Gómez, Juan C. Quintana, Patricia Arbeláez, Jorge Fernández, Juan F. Silva, Jacqueline Barona, Juan C. Gutiérrez, Abel Díaz, Rafael Otero, Picaduras por escorpión Tityus asthenes en Mutatá, Colombia: aspectos epidemiológicos, clínicos y toxinológicos , Biomédica: Vol. 30 Núm. 1 (2010)
- Juan Gabriel Piñeros, Malaria y determinantes sociales de la salud: un nuevo marco heurístico desde la medicina social latinoamericana , Biomédica: Vol. 30 Núm. 2 (2010)
- Angélica María Delgado-Vega, Javier Martín, Julio Granados, Juan Manuel Anaya, Epidemiología genética de la artritis reumatoide: ¿qué esperar de América Latina? , Biomédica: Vol. 26 Núm. 4 (2006)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























