El caseinato de sodio incrementa número de linfocitos B en ratones
Resumen
Introducción. El caseinato de sodio, una sal de la caseína utilizada como agente proinflamatorio en ratones, es capaz de inducir granulopoyesis en vivo e incrementar la producción de citocinas esenciales en dicho evento.
Objetivo. Evaluar si el caseinato de sodio es capaz de inducir un efecto biológico en células de origen linfoide y la producción de citocinas involucradas con este linaje.
Materiales y métodos: Se utilizaron ratones hembra BALB/c de 8 a 12 semanas de edad. Los animales se inyectaron cuatro veces, con intervalos de 48 horas, por vía intraperitoneal con 1 ml de caseinato de sodio (10 % de SFB p/v). La población de linfocitos B y la incorporación de bromodesoxiuridina (BrdU) se analizaron mediante citometría de flujo. La detección de la interleucina 7 se evaluó mediante la técnica de ELISA.
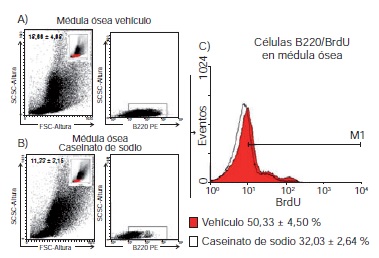
Resultados. Tras la inyección por vía intraperitoneal, el número de linfocitos B 220+ provenientes del bazo de ratones tratados con caseinato de sodio aumentó comparados con los que solo recibieron el vehículo como tratamiento (89,01±1,03 Vs. 75,66±2,08), así como la incorporación de BrdU en células B220+ (38,59±4,48 Vs. 11,82±1,04). Se evidenció, asimismo, el incremento en la concentración de la interleucina 7 (IL-7) en el suero de los ratones tratados con caseinato de sodio, comparados con los que solo recibieron el vehículo (62,1±17,5 Vs. 26,9±4,4 pg/ml).
Conclusión. El caseinato de sodio fue capaz de aumentar el número de linfocitos B en bazo de ratones, así como inducir la producción de IL-7, citocina clave para la linfopoyesis B.
Descargas
Referencias bibliográficas
Lotem J, Sachs L. Control of in vivo differentiation of myeloid leukemic cells. Leukemia. 1988;2:24s-37s.
Lotem J, Sachs L. Independent regulation of myeloid cell growth and differentiation inducing proteins: In vivo regulation by compounds that induce inflammation. Int J Cancer. 1985;35:93-100.
Santiago-Osorio E, Mora L, Bautista M, Montesinos JJ, Martínez I, Ramos-Mandujano G, et al. Sodium caseinate induces secretion of macrophage colony-stimulating factor from neutrophils. Immunobiology. 2010;215:332-9. https://doi.org/10.1016/j.imbio.2009.03.003
Córdova-Galaviz Y, Ledesma-Martínez E, Aguíñiga-Sánchez I, Soldevila-Melgarejo G, Soto-Cruz I, Weiss-Steider B, et al. Sodium caseinate induces increased survival in leukaemic mouse J774 model. In Vivo. 2014;28: 819-25.
Santiago-Osorio E, Ledesma-Martínez E, Aguiñiga-Sánchez I, Poblano-Pérez I, Weiss-Steider B, Montesinos-Montesinos JJ, et al. Sodium caseinate (CasNa) induces mobilization of hematopoietic stem cells in a BALB/c mouse model. Med Sci Monit Basic Res. 2015;21:206-12. https://doi.org/10.12659/MSMBR.895442
Domínguez-Meléndez V, Silvestre-Santana O, Moreno-Fierros L, Aguiñiga-Sánchez I, Martínez L, Marroquín-Segura R, et al. Sodium caseinate induces mouse granulopoiesis. Inflamm Res. 2012;61:367-73. https://doi.org/10.1007/s00011-011-0421-7
Metcalf D, Robb L, Dunn AR, Mifsud S, Di Rago L. Role of granulocyte-macrophage colony-stimulating factor and granulocyte colony stimulating factor in the development of an acute neutrophil inflammatory response in mice. Blood. 1996;88:3755-64.
Wong CW, Seow HF, Liu AH, Husband AJ, Smithers GW, Watson DL. Modulation of immune responses by bovine beta-casein. Immunol Cell Biol. 1996;74:323-9. https://doi.org/10.1038/icb.1996.58
Tobita K, Kawahara T, Otani H. Bovine beta-casein (1-28), a casein phosphopeptide, enhances proliferation and IL-6 expression of mouse CD19+ cells via Toll-like receptor 4. J Agric Food Chem. 2006;54:8013-7. https://doi.org/10.1021/jf0610864
Ma A, Koka R, Burkett P. Diverse functions of IL-2, IL-15, and IL-7 in lymphoid homeostasis. Annu Rev Immunol. 2006;24:657-79. https://doi.org/10.1146/annurev.immunol.24.021605.090727
Sitnicka E, Bryder D, Theilgaard-Mönch K, Buza-Vidas N, Adolfsson J, Jacobsen SE. Key role of flt3 ligand in regulation of the common lymphoid progenitor but not in maintenance of the hematopoietic stem cell pool. Immunity. 2002;17:463-72. https://doi.org/10.1016/S1074-7613(02)00419-3
Peschon JJ, Morrissey PJ, Grabstein KH, Ramsdell FJ, Maraskovsky E, Gliniak BC, et al. Early lymphocyte expansion is severely impaired in interleukin 7 receptor-deficient mice. J Exp Med. 1994;180:1955-60. https://doi.org/10.1084/jem.180.5.1955
Instituto de Biotecnología, Universidad Nacional Autónoma de México. Norma Oficial Mexicana NOM-062-ZOO-1999. Especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio. Fecha de consulta: 15 de enero de 2010. Disponible en: http://www.ibt.unam.mx/computo/pdfs/bioterio.NOM-062.pdf
Bertrand JY, Giroux S, Golub R, Klaine M, Jalil A, Boucontet L, et al. Characterization of purified intra-embryonic hematopoietic stem cells as a tool to define their site of origin. Proc Natl Acad Sci USA. 2005;102:134-9. https://doi.org/10.1073/pnas.0402270102
Cyster JG. Chemokines, sphingosine-1-phosphate, and cell migration in secondary lymphoid organs. Annu Rev Immunol. 2005;23:127-59. https://doi.org/10.1146/annurev.immunol.23.021704.115628
Fu YX, Chaplin DD. Development and maturation of secondary lymphoid tissues. Annu Rev Immunol. 1999;17: 399-433. https://doi.org/10.1146/annurev.immunol.17.1.399
Dias S, Silva H Jr, Cumano A, Vieira P. Interleukin-7 is necessary to maintain the B cell potential in common lymphoid progenitors. J Exp Med. 2005;201:971-9. https://doi.org/10.1084/jem.20042393
Milne CD, Paige CJ. IL-7: A key regulator of B lympho-poiesis. Semin Immunol. 2006;18:20-30. https://doi.org/10. 1016/j.smim.2005.10.003
Ueda Y, Yang K, Foster SJ, Kondo M, Kelsoe G. Inflam-mation controls B lymphopoiesis by regulating chemokine CXCL12 expression. J Exp Med. 2004;199:47-58. https://doi.org/10.1084/jem.20031104
Ueda Y, Kondo M, Kelsoe G. Inflammation and the reciprocal production of granulocytes and lymphocytes in bone marrow. J Exp Med. 2005;201:1771-80. https://doi.org/10.1084/jem.20041419
von Freeden-Jeffry U, Vieira P, Lucian LA, McNeil T, Burdach SE, Murray R. Lymphopenia in interleukin (IL)-7 gene-deleted mice identifies IL-7 as a nonredundant cytokine. J Exp Med. 1995;181:1519-26. https://doi.org/10. 1084/jem.181.4.1519
Morrison SJ, Wright DE, Weissman IL. Cyclophosphamide/granulocyte colony-stimulating factor induces hematopoietic stem cells to proliferate prior to mobilization. Proc Natl Acad Sci USA. 1997;94:1908-13
Inra CN, Zhou BO, Acar M, Murphy MM, Richardson J, Zhao Z, et al. A perisinusoidal niche for extramedullary haematopoiesis in the spleen. Nature. 2015;26:466-71. https://doi.org/10.1038/nature15530
Algunos artículos similares:
- Luis A. Franco, Germán E. Matiz, Jairo Calle, Roberto Pinzón, Luis F. Ospina, Actividad antinflamatoria de extractos y fracciones obtenidas de cálices de Physalis peruviana L. , Biomédica: Vol. 27 Núm. 1 (2007)
- Ana María Vásquez, Alberto Tobón, Mecanismos de patogenia en la malaria por Plasmodium falciparum , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Luis Ángel Villar, Rosa Margarita Gélvez, Jairo Antonio Rodríguez, Doris Salgado, Beatriz Parra, Lyda Osorio, Irene Bosch, Biomarcadores pronósticos de gravedad del dengue , Biomédica: Vol. 33 (2013): Suplemento 1, Fiebres hemorrágicas
- Wilson Mejía-Naranjo, Myriam Sánchez-Gomez, La desnutrición proteica estimula la expresión de receptores de la hormona del crecimiento en linfocitos B esplénicos de rata , Biomédica: Vol. 24 Núm. 4 (2004)
- Adriana Cuéllar, Angela Fonseca, Alberto Gómez, Efecto del lipopolisacárido en cultivos de células dendríticas humanas y su inhibición por la polimixina B. , Biomédica: Vol. 24 Núm. 4 (2004)
- Fabián Jaimes, Gisela de la Rosa, Anticoagulación y sepsis, la oportunidad para un nuevo uso de la heparina? , Biomédica: Vol. 26 Núm. 1 (2006)
- Clelia Rosa Calao, José Luis Marrugo, Efectos genotóxicos asociados a metales pesados en una población humana de la región de La Mojana, Colombia, 2013 , Biomédica: Vol. 35 (2015): Agosto, Suplemento 2, Salud y contaminantes ambientales
- Henry A. Vargas, Martín Rondón, Rodolfo Dennis, Tipo de tratamiento farmacológico y deterioro de la función pulmonar en pacientes con diabetes tipo 2: un estudio de corte transversal , Biomédica: Vol. 36 Núm. 2 (2016)
- Tania Yadira Martínez-Rodríguez, Mauricio Rey-Buitrago, Expresión de alfa sinucleína en sangre y su relación con el estreñimiento crónico en población residente en Bogotá, D.C., con problemas de consumo de alcohol , Biomédica: Vol. 40 Núm. 2 (2020)
- Concepción Sánchez-Martínez , Liliana Torres-González , Gabriela Alarcón-Galván , Linda E. Muñoz-Espinosa , Homero Zapata-Chavira , Diana Patricia Moreno-Peña, Homero Náñez-Terreros, Edelmiro Pérez-Rodríguez , Lourdes Garza-Ocañas , Francisco Javier Guzmán-de la Garza , Paula Andrea Cordero, Actividad antiinflamatoria y antioxidante de los α-cetoanálogos de aminoácidos esenciales en un modelo de daño por isquemia-reperfusión en ratas Wistar , Biomédica: Vol. 40 Núm. 2 (2020)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























