Criptococosis meníngea e infección por SARS-CoV-2 en personas con VIH/SIDA
Resumen
Introducción. Las infecciones fúngicas en pacientes con COVID-19 fue uno de los temas más debatidos durante la pandemia.
Objetivo. Analizar las características clínicas y la evolución de personas con VIH/SIDA que presentaron la asociación de criptococosis meníngea y COVID-19 (grupo A), y compararlas con aquellas personas con VIH/SIDA que padecieron criptococosis meníngea, pero sin infección de COVID-19 (grupo B).
Materiales y métodos. Se realizó un estudio analítico y retrospectivo en el que se revisaron las historias clínicas de pacientes que padecieron criptococosis meníngea entre abril de 2020 y mayo de 2021.
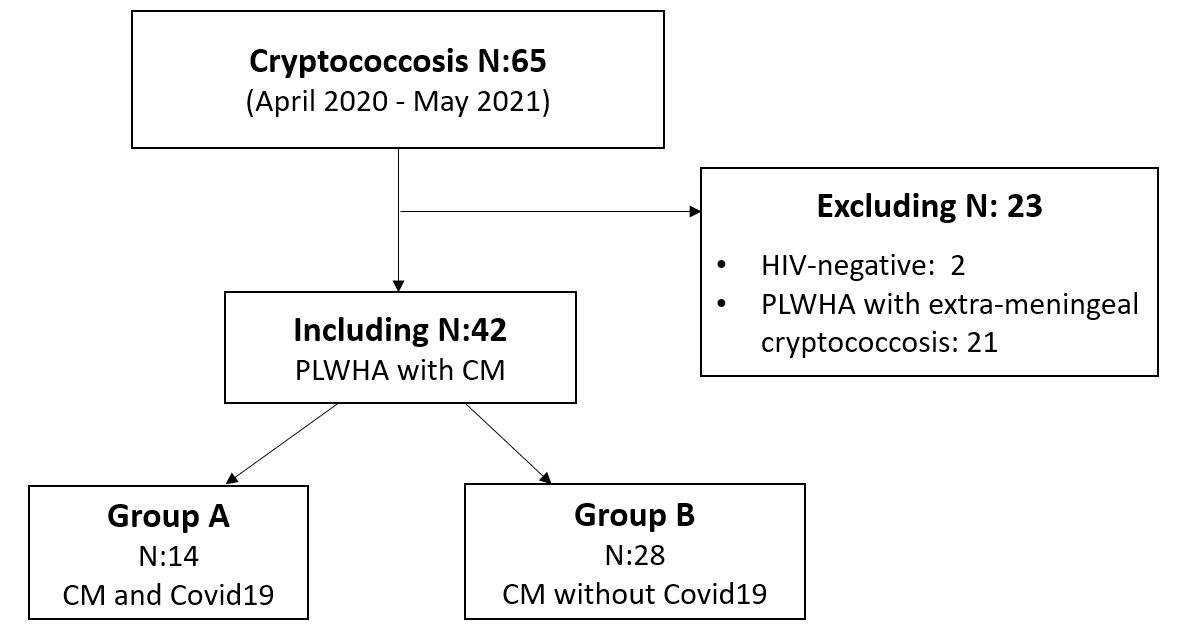
Resultados. Se estudiaron 65 pacientes con HIV/SIDA y con criptococosis, diagnosticados entre abril de 2020 y mayo de 2021 (63 habían desarrollado sida y 2 eran negativos para VIH). De estos, 15 de los pacientes con sida padecían criptococosis y COVID-19, y 14 presentaban meningitis (grupo A), mientras que 28 pacientes padecieron criptococosis meníngea, pero no tuvieron COVID-19 (grupo B).
Conclusiones. No se observaron diferencias estadísticamente significativas, entre los dos grupos, respecto a la hipertensión intracraneal, la presencia de antígenos de criptoccoco en líquido cefalorraquídeo, el deterioro del sensorio o la mortalidad. La detección de antígenos de Cryptococcus en suero por ensayo de flujo lateral fue efectiva para diagnosticar rápidamente criptococosis en personas con VIH/sida y con infección de COVID-19. Se observó que los pacientes de ambos grupos consultaron tarde por criptococosis en comparación con los casos prepandémicos de esta infección.
Descargas
Referencias bibliográficas
Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med. 2020;382:727-33. https://doi.org/10.1056/NEJMoa2001017
Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020;395:497-506. https://doi.org/10.1016/S0140-6736(20)30183-5
Cucinotta D, Vanelli M. WHO declares COVID-19 a pandemic. Acta Biomed. 2020;91:157-60. https://doi.org/10.23750 /abm.v91i1.9397
Zhang H, Wu T. CD4+T, CD8+T counts and severe COVID-19: A meta-analysis. J Infect. 2020;81:e82-e4. https://doi.org/10.1016/j.jinf.2020.06.036
Ho HE, Peluso MJ, Margus C, Matias Lopes JP, He C, Gaisa MM, et al. Clinical outcomes and immunologic characteristics of coronavirus disease 2019 in people with human immunodeficiency virus. J Infect Dis. 2021;223:4038. https://doi.org/10.1093/infdis/jiaa380
Lee KW, Yap SF, Ngeow YF, Lye MS. COVID-19 in people living with HIV: A systematic review and meta-analysis. Int J Environ Res Public Health. 2021;18:3554. https://doi.org/10.3390/ijerph18073554
Pal R, Singh B, Bhadada SK, Banerjee M, Bhogal RS, Hage N, et al. COVID-19-associated mucormycosis: An updated systematic review of literature. Mycoses. 2021;64:1452-9. https://doi.org/10.1111/myc.13338
Kariyawasam RM, Dingle TC, Kula BE, Vandermeer B, Sligl WI, Schwartz IS. Defining COVID-19-associated pulmonary aspergillosis: Systematic review and meta-analysis. Clin Microbiol Infect. 2022;28:920-7. https://doi.org/10.1016/j.cmi.2022.01.027
Messina F, Marin E, Valerga M, Depardo R, Chediak V, Romero M et al. Updates on AIDS and infectology. Actualizaciones en Sida e Infectología. 2021;29:6-16. https://doi.org/10.52226/revista.v29i105.49
Khatib MY, Ahmed AA, Shaat SB, Mohamed AS, Nashwan AJ. Cryptococcemia in a patient with COVID-19: A case report. Clin Case Rep. 2020;9:853-5. https://doi.org/10.1002/ccr3.3668
Woldie IL, Brown IG, Nwadiaro NF, Patel A, Jarrar M, Quint E, et al. Autoimmune hemolytic anemia in a 24-year-old patient with COVID-19 complicated by secondary cryptococcemia and acute necrotizing encephalitis: A case report and review of literature. J Med Cases. 2020;11:362-5. https://doi.org/10.14740/jmc3575
Frías-De-León MG, Pinto-Almazán R, Hernández-Castro R, GarcíaSalazar E, Meza-Meneses P, Rodríguez-Cerdeira C, et al. Epidemiology of systemic mycoses in the COVID-19 pandemic. J Fungi (Basel). 2021;7:556. https://doi.org/10.3390/jof7070556
Arechavala A, Negroni R, Messina F, Romero M, Marín E, Depardo R, et al. Cryptococcosis in an infectious diseases hospital of Buenos Aires, Argentina. Revision of 2041 cases: Diagnosis, clinical features and therapeutics. Rev Iberoam Micol. 2018;35:1-10. https://doi.org/10.1016/j.riam.2017.04.003
Firacative C, Meyer W, Castañeda E. Cryptococcus neoformans and Cryptococcus gatti species complexes in Latin America: A map of molecular types, genotypic diversity, and antifungal susceptibility as reported by the Latin American Cryptococcal Study Group. J Fungi (Basel). 2021;7:282. https://doi.org/10.3390/jof7040282
Rajasingham R, Govender NP, Jordan A, Loyse A, Shroufi A, Denning DW, et al. The global burden of HIV-associated cryptococcal infection in adults in 2020: a modelling analysis. Lancet Infect Dis. 2022;22:1748-55. https://doi.org/10.1016/S1473-3099(22)00499-6
Guelfand L, Cataldi S, Arechavala A, Perrone M. Manual práctico de micología médica. Acta Bioquim Clin Latinoam. 2015; Supl. 1.
Arechavala AI, Robles AM, Negroni R, Bianchi MH, Taborda A. Value of direct and indirect diagnostic methods in systemic mycoses associated with AIDS. Rev Inst Med Trop Sao Paulo. 1993;35:163-9. https://doi.org/10.1590/s0036-46651993000200008
Huang HR, Fan LC, Rajbanshi B, Xu JF. Evaluation of a new cryptococcal antigen lateral flow immunoassay in serum, cerebrospinal fluid and urine for the diagnosis of cryptococcosis: A meta-analysis and systematic review. PLoS One. 2015;10:e0127117. https://doi.org/10.1371/journal.pone.0127117
IMMY. Immy CrAg lateral flow assay REF CR2003. Fecha de consulta: 05 de agosto del 2020. Disponible en: www.immy.com
Centers for Disease Control and Prevention. Cryptococcal screening a new strategy for saving lives among people with HIV/AIDS 11-10-2021. Fecha de consulta: 12 de octubre del 2020: Disponible en: https://www.cdc.gov/fungal/pdf/crypto-screen-strategy-508c.pdf
Hu B, Guo H, Zhou P, Shi ZL. Characteristics of SARS-CoV-2 and COVID-19. Nat Rev Microbiol. 2021;19:141-54. https://doi.org/10.1038/s41579-020-00459-7. Erratum in: Nat Rev Microbiol. 2022 May;20:315.
Messina FA, Maiolo E, Negroni R, Arechavala A, Santiso G, Bianchi M. Alternativas terapéuticas de la criptococosis meníngea. ASEI. 2015;23:2532.
Liu J, Li H, Luo M, Liu J, Wu L, Lin X, et al. Lymphopenia predicted illness severity and recovery in patients with COVID-19: A single-center, retrospective study. PLoS One. 2020;15:e0241659. https://doi.org/10.1371/journal.pone.0241659
Toori KU, Qureshi MA, Chaudhry A. Lymphopenia: A useful predictor of COVID-19 disease severity and mortality. Pak J Med Sci. 2021;37:1984-8. https://doi.org/10.12669/pjms.37.7.4085
Sayah W, Berkane I, Guermache I, Sabri M, Lakhal FZ, Yasmine Rahali S, et al. Interleukin-6, procalcitonin and neutrophil-to-lymphocyte ratio: Potential immuneinflammatory parameters to identify severe and fatal forms of COVID-19. Cytokine. 2021;141:155428. https://doi.org/10.1016/j.cyto.2021.155428
Regalla D, VanNatta M, Alam M, Malek AE. COVID-19-associated Cryptococcus infection (CACI): a review of literature and clinical pearls Infection. 2022;50:1-6. https://doi.org/10.1007/s15010-022-01805-y
Algunos artículos similares:
- Carolina Firacative, Germán Torres, María Claudia Rodríguez, Patricia Escandón, Primer aislamiento ambiental de Cryptococcus gattii de serotipo B, en Cúcuta, Colombia , Biomédica: Vol. 31 Núm. 1 (2011)
- Daniel Echeverri, María de los Ángeles Vargas, Lorena Matta, Fernando Rosso, Janier Daniel Segura, Infección invasiva por Streptococcus pneumoniae: reporte de caso de un paciente con síndrome de Austrian , Biomédica: Vol. 35 Núm. 1 (2015)
- Jairo Lizarazo, Edgar Parra, Patricia Gutiérrez, Carlos Mora, Juan Vargas, Paquimeningitis craneal hipertrófica idiopática. , Biomédica: Vol. 24 Núm. 2 (2004)
- Patricia Escandón, Elizabeth Quintero, Diana Granados, Sandra Huérfano, Alejandro Ruiz, Elizabeth Castañeda, Aislamiento de Cryptococcus gattii serotipo B a partir de detritos de Eucalyptus spp. en Colombia. , Biomédica: Vol. 25 Núm. 3 (2005)
- Clara Inés Agudelo, Jaime Moreno, Olga Marina Sanabria, María Victoria Ovalle, José Luis Di Fabio, Elizabeth Castañeda, Streptococcus pneumoniae: evolución de los serotipos y los patrones de susceptibilidad antimicrobiana en aislamientos invasores en 11 años de vigilancia en colombia (1994 -2004). , Biomédica: Vol. 26 Núm. 2 (2006)
- Carolina Firacative, Jaime Moreno, Elizabeth Castañeda, Caracterización molecular de aislamientos invasores colombianos de Streptococcus pneumoniae serotipo 5 recuperados entre 1994 y 2004. , Biomédica: Vol. 26 Núm. 2 (2006)
- Claudia Calderón, Rodolfo Dennis, Costos económicos de neumonía adquirida en comunidad, meningitis y bacteriemia por Streptococcus pneumoniae en una población adulta que requirió hospitalización en Bogotá, Colombia , Biomédica: Vol. 34 Núm. 1 (2014)
- Natalia Osorio, Yúrika López, Juan Camilo Jaramillo, Histoplasmosis del sistema nervioso central en un paciente inmunocompetente , Biomédica: Vol. 34 Núm. 4 (2014)
- Jaime Moreno, Olga Sanabria, Sandra Saavedra, Karina Rodríguez, Carolina Duarte, Caracterización fenotípica y genotípica de aislamientos de Neisseria meningitidis, serogrupo B, procedentes de Cartagena, Colombia, 2012-2014 , Biomédica: Vol. 35 Núm. 1 (2015)
- Claudia Castro, Alba Ricardo, Angie Zabaleta, Claudia Llerena, Gloria Puerto, Caracterización de aislamientos clínicos de Mycobacterium tuberculosis obtenidos de individuos positivos para HIV en Colombia, 2012 , Biomédica: Vol. 37 Núm. 1 (2017)
Derechos de autor 2023 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























