Caracterización molecular del dominio de la hélice del gen k13 de Plasmodium falciparum en muestras de comunidades nativas de Condorcanqui, Amazonas, Perú
Resumen
Introducción. La resistencia de Plasmodium falciparum a diferentes fármacos antipalúdicos es un obstáculo para eliminar la enfermedad. El genotipo resistente de P. falciparum a la artemisinina puede evaluarse examinando los polimorfismos en el dominio de la hélice del gen Pfk13. La Organización Mundial de la Salud recomienda utilizar estas mutaciones como marcadores moleculares para detectar la resistencia a la artemisinina en países donde la malaria por P. falciparum es endémica.
Objetivo. Identificar mutaciones relacionadas con la resistencia a artemisinina presentes en el dominio de la hélice del gen k13 de P. falciparum.
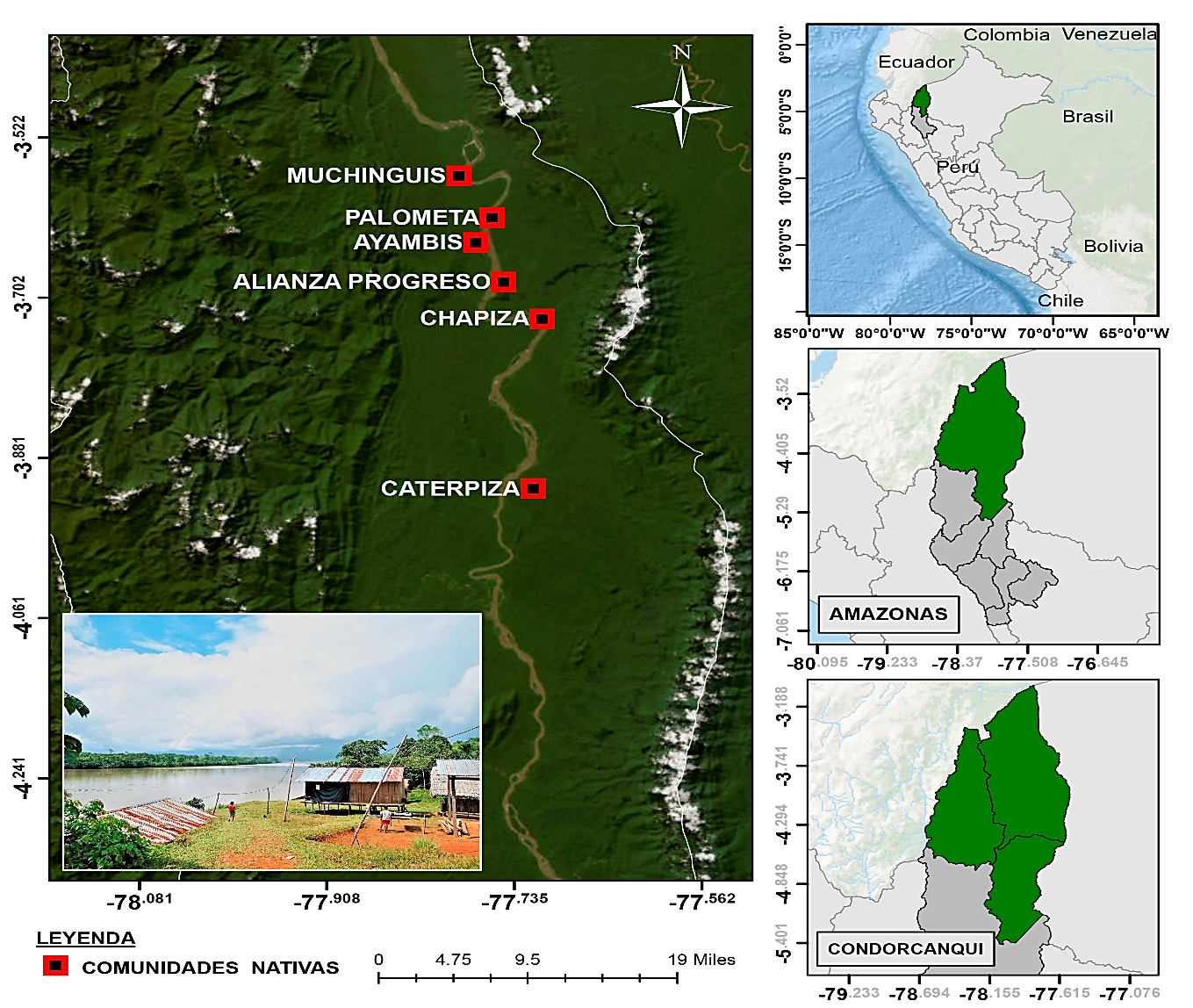
Materiales y métodos. Mediante la detección pasiva de casos, se recolectaron 51 muestras positivas por microscopía para Plasmodium, provenientes de seis comunidades del distrito de Río Santiago en Condorcanqui, Amazonas. Se realizó la confirmación molecular de la especie mediante PCR en tiempo real y el dominio de la hélice del gen Pfk13 se amplificó y secuenció por electroforesis capilar. Las secuencias obtenidas se compararon con la cepa de referencia 3D7 de fenotipo silvestre.
Resultados. Se confirmó un total de 51 muestras positivas para P. falciparum, provenientes de las comunidades de Ayambis, Chapiza, Palometa, Muchinguis, Alianza Progreso y Caterpiza. Después del alineamiento de las secuencias de ADN, se determinó que las muestras no presentaron mutaciones asociadas con resistencia en el gen K13.
Discusión. Los resultados obtenidos son coherentes con estudios similares realizados en otros países de Sudamérica, incluyendo Perú. Estos datos proporcionan una línea base para la vigilancia molecular de resistencia a artemisinina en la región Amazonas y refuerzan la eficacia de la terapia combinada con artemisinina en esta área.
Descargas
Referencias bibliográficas
Chapadense F, Machado RL, Ventura AMR da S, Áreas A, Machado RB, Viana GR, et al. Plasmodium falciparum malarial parasites from Brazil lack artemisinin resistance-associated mutations in the kelch13 gene. Soc Bras Med Trop. 2019;52:e20180225. https://doi.org/10.1590/0037-8682-0225-2018
Valenzuela G, Castro LE, Valencia-Zamora J, Vera-Arias CA, Rohrbach P, Sáenz FE. Genotypes and phenotypes of resistance in Ecuadorian Plasmodium falciparum. Malar J. 2019;18:415. https://doi.org/10.1186/s12936-019-3044-z
Mathieu LC, Cox H, Early AM, Mok S, Lazrek Y, Paquet J, et al. Local emergence in Amazonia of Plasmodium falciparum K13 C580Y mutants associated with in vitro artemisinin resistance. eLife. 2020;9:e51015. https://doi.org/10.7554/eLife.51015
Boullé M, Witkowski B, Duru V, Sriprawat K, Nair SK, McDew-White M, et al. Artemisininresistant Plasmodium falciparum K13 mutant alleles, Thailand–Myanmar border. Emerg Infect Dis. 2016;22:1503-5. https://doi.org/10.3201/eid2208.160004
Gomes LR, Lavigne A, Peterka CL, Brasil P, Ménard D, Daniel-Ribeiro CT, et al. Absence of K13 polymorphism in Plasmodium falciparum from Brazilian areas where the parasite is endemic. Antimicrob Agents Chemother. 2018;62:e00354-18. https://doi.org/10.1128/AAC.00354-18
Ghanchi NK, Qurashi B, Raees H, Beg MA. Molecular surveillance of drug resistance: Plasmodium falciparum artemisinin resistance single nucleotide polymorphisms in Kelch protein propeller (K13) domain from Southern Pakistan. Malar J. 2021;20:176. https://doi.org/10.1186/s12936-021-03715-0
Kamau E, Campino S, Amenga-Etego L, Drury E, Ishengoma D, Johnson K, et al. K13-propeller polymorphisms in Plasmodium falciparum parasites from sub-Saharan Africa. J Infect Dis. 2015;211:1352-5. https://doi.org/10.1093/infdis/jiu608
Chenet SM, Akinyi-Okoth S, Huber CS, Chandrabose J, Lucchi NW, Talundzic E, et al. Independent emergence of the Plasmodium falciparum Kelch propeller domain mutant allele C580Y in Guyana. J Infect Dis. 2016;213:1472-5. https://doi.org/10.1093/infdis/jiv752
Arróspide N, Hijar-Guerra G, De Mora D, Díaz-Cortéz CE, Veloz-Pérez R, Gutiérrez S, et al. Alelos mutantes asociados a la resistencia a cloroquina y sulfadoxina-pirimetamina en Plasmodium falciparum de las fronteras Ecuador-Perú y Ecuador-Colombia. Rev Peru Med Exp Salud Publica. 2014;31:282-7.
Williams HA, Vincent-Mark A, Herrera Y, Chang OJ. A retrospective analysis of the change in anti-malarial treatment policy: Peru. Malar J. 2009;8:85. https://doi.org/10.1186/1475-2875-8-85
Ministerio de Salud del Perú. Norma técnica de salud para la atención de la malaria y malaria grave en el Perú. Lima: Ministerio de Salud; 2015.
World Health Organization. Good manufacturing practices for sterile pharmaceutical products. Ginebra: WHO; 2004. Fecha de consulta: 5 de mayo de 2023. Disponible en: https://www.who.int/es/publications/i/item/HTM-GMP-MM-SOP-10
Montenegro CC, Bustamante-Chauca TP, Pajuelo-Reyes C, Bernal M, Gonzales L, Tapia-Limonchi R, et al. Plasmodium falciparum outbreak in native communities of Condorcanqui, Amazonas, Perú. Malar J. 2021;20:88. https://doi.org/10.1186/s12936-021-03608-2
Rougemont M, van Saanen M, Sahli R, Hinrikson HP, Bille J, Jaton K. Detection of four Plasmodium species in blood from humans by 18S rRNA gene subunit-based and speciesspecific real-time PCR assays. J Clin Microbiol. 2004;42:5636-43. https://doi.org/10.1128/JCM.42.12.5636-5643.2004
Yasri S, Wiwanitkit V. Artemisinin resistance: An important emerging clinical problem in tropical medicine. Int J Physiol Pathophysiol Pharmacol. 2021;13:152-7.
Montenegro LM, de Las Salas B, Neal AT, Tobon-Castaño A, Fairhurst RM, Lopera-Mesa TM. State of artemisinin and partner drug susceptibility in Plasmodium falciparum clinical isolates from Colombia. Am J Trop Med Hyg. 2021;104:263-70. https://doi.org/10.4269/ajtmh.20-0148
Inoue J, Jovel I, Morris U, Aydin-Schmidt B, Islam A, Segurado AC, et al. Absence of Plasmodium falciparum K13 propeller domain polymorphisms among field isolates collected from the Brazilian Amazon Basin between 1984 and 2011. Am J Trop Med Hyg. 2018;99:1504-7. https://doi.org/10.4269/ajtmh.18-05541504
Gomes LR, Lavigne A, Peterka CL, Brasil P, Ménard D, Daniel-Ribeiro CT, et al. Absence of K13 polymorphism in Plasmodium falciparum from Brazilian areas where the parasite is endemic. Antimicrob Agents Chemother. 2018;62:e00354-18. https://doi.org/10.1128/AAC.00354-18
Villena FE, Sánchez JF, Nolasco O, Braga G, Ricopa L, Barazorda K, et al. Drug resistance and population structure of Plasmodium falciparum and Plasmodium vivax in the Peruvian Amazon. Sci Rep. 2022;12:16474. https://doi.org/10.1038/s41598-022-21028-3
Kattenberg JH, Fernández-Miñope C, van Dijk NJ, Llacsahuanga-Allcca L, Guetens P, Valdivia HO, et al. Malaria molecular surveillance in the Peruvian Amazon with a novel highly multiplexed Plasmodium falciparum AmpliSeq assay. Microbiol Spectr. 2023;11:e0096022. https://doi.org/10.1128/spectrum.00960-22
Rawat M, Kanyal A, Choubey D, Deshmukh B, Malhotra R, Mamatharani DV, et al. Identification of co-existing mutations and gene expression trends associated with K13-mediated artemisinin resistance in Plasmodium falciparum. Front Genet. 2022;13:824483. https://doi.org/10.3389/fgene.2022.824483
Oberstaller J, Zoungrana L, Bannerman CD, Jahangiri S, Dwivedi A, Silva JC, et al. Integration of population and functional genomics to understand mechanisms of artemisinin resistance in Plasmodium falciparum. Int J Parasitol Drugs Drug Resist. 2021;16:119-28. https://doi.org/10.1016/j.ijpddr.2021.05.006
Ministerio de Salud del Perú. Plan hacia la eliminación de la Malaria en el Perú 2022-2030. Lima: Ministerio de Salud del Perú; 2022.
Algunos artículos similares:
- Eliana P. Calvo, María O. Rojas, Jacqueline Chaparro, Moisés Wasserman, Expresión del gen asociado con la resistencia múltiple a medicamentos (pfmdrl) en cepas colombianas de Plasmodium falciparum , Biomédica: Vol. 19 Núm. 3 (1999)
- Iveth J. González, Las metacaspasas y su rol en la vida y muerte de los parásitos protozoarios humanos , Biomédica: Vol. 29 Núm. 3 (2009)
- Carolina Montoya, Priscila Bascuñán, Julián Rodríguez-Zabala, Margarita M. Correa, Abundancia, composición e infección natural de mosquitos Anopheles en dos regiones endémicas para malaria en Colombia , Biomédica: Vol. 37 Núm. Sup. 2 (2017): Suplemento 2, Entomología médica, 2017
- César Segura, Silvia Blair, La mitocondria en el género Plasmodium. , Biomédica: Vol. 23 Núm. 3 (2003)
- Andrés Fernando Rodríguez-Gutiérrez, Isabel Cristina Ramírez-Sánchez, Malaria después de trasplante hepático: reporte de dos casos y revisión de los casos publicados , Biomédica: Vol. 45 Núm. 2 (2025)
- Nancy Arrospide, Hernán Sanabria, William J. Araujo-Banchon, Evaluación de la efectividad de la prueba rápida OptiMAL-IT™ para el seguimiento de pacientes con diagnóstico de malaria en la Amazonía peruana , Biomédica: Vol. 42 Núm. 1 (2022)
- Pamela Orjuela, Iveth González, Lyda Osorio, Terapia combinada como estrategia en la prevención de la resistencia a los antimaláricos. , Biomédica: Vol. 24 Núm. 4 (2004)
- Elizabeth Borrero, Gabriel Carrasquilla, Neal Alexander, Descentralización y reforma: ¿cuál es su impacto sobre la incidencia de malaria en los municipios colombianos? , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Pablo Chaparro, Edison Soto, Julio Padilla, Daniel Vargas, Estimación del subregistro de casos de paludismo en diez municipios de la costa del Pacífico nariñense durante 2009 , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Julio Cesar Padilla-Rodríguez , Mario J. Olivera, Evaluación de costos y resultados de la Campaña de Erradicación de la Malaria en Colombia entre 1957 y 1969 , Biomédica: Vol. 45 Núm. 3 (2025)
Derechos de autor 2023 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























