Risk of transmission of Chagas disease by intrusion of triatomines and wild mammals in Bucaramanga, Santander, Colombia
Abstract
Introduction: Notice of triatomines in dwellings of some neighborhoods in Bucaramanga motivated the realization of this study.
Objetive: To evaluate the intrusion of triatomines and mammals, as well as some risk factors in urban dwellings.
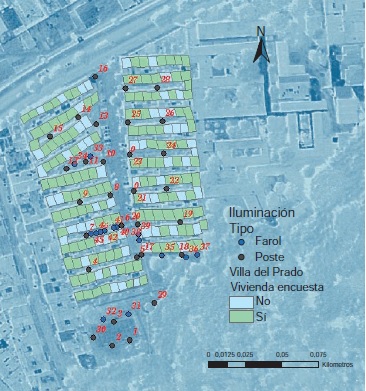
Materials and methods: Triatomines were collected in a neighborhood in Bucaramanga, Santander, on a monthly basis during one year with participation of the community. Collection included manual search in lamp posts, use of light traps, animal bait, and chemical attractants in nearby forests. Reservoirs were collected with bait traps. Insects and mammals were identified and examined in order to determine their natural infection. Risk factors in homes were assessed by means of a social-environmental survey.
Results: Eleven adult specimens of Pastrongylus geniculatus, as well as 63 of Rhodnius pallescens were collected in the forest, recreational peridomiciliary areas, and houses. Even two females and 21 nymphs of R. pallescens were found in bedrooms. Two specimens of Didelphis marsupialis were captured in neighboring forests. Out of the eleven P. geniculatus captured, nine were examined. Of these, five were positive for Trypanosoma cruzi. It was not possible to establish a significant risk factor;
however, the dwellings with report of triatomines were located nearer to the adjacent forest.
Conclusions: The finding of intrusive triatominae species and mammals with T. cruzi in intradomiciliary and peridomiciliary areas and periurban forests prove the potential risk to acquire infection from these populations that dwell in urban housing adjacent to these ecotopes where the sylvan cycle is kept.
Downloads
References
World Health Organization. Chagas disease in Latin America: An epidemiological update based on 2010 estimates. Wkly Epidemiol Rec. 2015;6:33-44.
Padilla JC. Situación de la enfermedad de Chagas en Colombia. En: Guhl F, editor. Primer Taller Internacional sobre Control de la Enfermedad de Chagas. Bogotá: Universidad de los Andes; 2005. p. 19-24.
Ministerio de la Protección Social, Instituto Nacional de Salud, Organización Panamericana de la Salud. Guía. Protocolo para la vigilancia en salud pública de Chagas. Bogotá: Ministerio de la Protección Social-INS; 2010.
Díaz ML, González CI. Enfermedad de Chagas agudo: transmisión oral de Trypanosoma cruzi como una vía de transmisión re-emergente. Rev Univ Ind Santander Salud. 2014;46:177-88.
Rueda K, Trujillo JE, Carranza JC, Vallejo GA. Transmisión oral de Trypanosoma cruzi: una nueva situación epidemiológica de la enfermedad de Chagas en Colombia y otros países suramericanos. Biomédica. 2014;34:631-41. http://dx.doi.org/10.7705/biomedica.v34i4.2204
Ríos J, Arboleda, M, Montoya AN, Alarcón EP, Parra GJ. Probable brote de transmisión oral de enfermedad de Chagas en Turbo, Antioquia. Biomédica. 2011;31:185-95.
http://dx.doi.org/10.7705/biomedica.v31i2.302
Briceño-León R, Méndez-Galván J. The social determinants of Chagas disease and the transformations of Latin America. Mem Inst Oswaldo Cruz. 2007;102:109-12. http://dx.doi.org/10.1590/S0074-02762007005000095
Borges EC, Dujardin, JP, Schofield CJ, Romanha AJ, Diotaiuti L. Dynamics between sylvatic, peridomestic and domestic populations of Triatoma brasiliensis (Hemiptera: Reduviidae) in Ceara state, Northeastern Brazil. Acta Trop. 2005;93:119-26. http://dx.doi.org/10.1016/j.actatropica.2004.10.002
Angulo VM. Aspectos ecológicos de la enfermedad de Chagas en el oriente de Colombia. MVZ Córdoba. 2000;5:64-8.
Herrera L. Una revisión sobre reservorios de Trypanosoma (Schizotrypanum) cruzi (Chagas, 1909), agente etiológico de la enfermedad de Chagas. Bol Mal Salud Amb. 2010;50:3-15.
Valente S, Valente V, Neto H. Considerations on the epidemiology and transmission of Chagas disease in the Brazilian Amazon. Mem Inst Oswaldo Cruz. 1999;94:395-8. http://dx.doi.org/10.1590/S0074-02761999000700077
Travi B, Jaramillo C, Montoya J, Segura I, Zea A, Gonçalves A, et al. Didelphis marsupialis, an important reservoir of Trypanosoma (Schizotrypanum) cruzi and Leishmania (Leishmania) chagasi in Colombia. Am J Trop Med Hyg. 1994;50:557-61.
Ramírez JD, Montilla M, Cucunubá-Pérez ZM, Flórez AC, Zambrano P, Guhl F. Molecular epidemiology of human oral Chagas disease outbreaks in Colombia. PLoS Negl Trop Dis. 2013;7:e2041. http://dx.doi.org/10.1371/journal.pntd.0002041
Mundaray O, Palomo N, Querales M, De Lima A R, Contreras V, Graterol D, et al. Factores de riesgo, nivel de conocimiento y seroprevalencia de enfermedad de Chagas en el municipio San Diego, Estado Carabobo. Venezuela. Salus. 2013;17:24-8.
Hurtado LA, Calzada JE, Pineda V, González K, Santamaría AM, Cáceres L, et al. Conocimientos y factores de riesgo relacionados con la enfermedad de Chagas en dos comunidades panameñas donde Rhodnius pallescens es el vector principal. Biomédica. 2014;34:260-70. http://dx.doi.org/10.7705/biomedica.v34i2.2133
Sanmartino M, Crocco L. Conocimientos sobre la enfermedad de Chagas y factores de riesgo en comunidades epidemiológicamente diferentes de Argentina. Rev Panam Salud Pública. 2000;7:173-8. http://dx.doi.org/10.1590/S1020-49892000000300006
Javit M, Traviezo V, Rodríguez L, Perdomo R. Hallazgo de Panstrongylus geniculatus en urbanización de la zona este de Barquisimeto, estado Lara, Venezuela. REDVET. 2012;13:1-10.
Reyes-Lugo M. Panstrongylus geniculatus Latreille 1811 (Hemiptera : Reduviidae : Triatominae), vector de la enfermedad de Chagas en el ambiente domiciliario del centronorte de Venezuela. Rev Biomed. 2009;20:180-205.
Carrasco HJ, Torrellas A, García C, Segovia M, Feliciangeli MD. Risk of Trypanosoma cruzi I (Kinetoplastida: Trypanosomatidae) transmission by Panstrongylus geniculatus (Hemiptera: Reduviidae) in Caracas (Metropolitan District) and neighboring states, Venezuela. Int J Parasitol. 2005;35:1379-84. http://dx.doi.org/10.1016/j.ijpara.2005.05.003
Wolff M, Castillo D. Evidencias de domesticación y aspectos biológicos de Panstrogylus geniculatus (Latrelle, 1881) (Hemiptera: Reduviidae). Acta Entomol Chilena. 2000;24:77-83.
Wolff M, González C. Ciclo de vida de Panstrongylus geniculatus (Hemiptera: Reduviidae) en condiciones de laboratorio. Caldasia. 1998;1:75-7.
Carcavallo R, Rodríguez ME, Salvatella R, Curto de Casas SI, Sherlock IS, Galvão C, et al. Habitats and related fauna. In: Carcavallo RU, Galíndez Girón I, Jurberg J, Lent H, editors. Atlas of Chagas’ disease vectors in the Americas. Rio de Janeiro: Editora Fiocruz; 1998. p. 561-600.
Lent H, Wygodzinsky P. Revision of the Triatominae (Hemiptera, Reduviidae), and their significance as vectors of Chagas disease. Bull Am Mus Nat Hist. 1979;163:123-520.
Leite G, dos Santos C, Falqueto A. Insecta, Hemiptera, Reduviidae, Panstrongylus geniculatus: Geographic distribution map. Check List. 2007;3:147-52.
Flórez M, Angulo VM. Cría masiva y uso de ninfas de Rhodnius pallescens, Barber, 1932 (Hemiptera, Reduviidae, Triatominae) para ensayos biológicos. Rev Univ Ind Santander Salud. 2015;47:15-22.
Organización Panamericana de la Salud. Taller técnico de estudio sobre Rhodnius pallescens, su vigilancia y control. Panamá: OPS; 2002.
Angulo VM, Esteban L. Nueva trampa para la captura de triatominos en hábitats silvestres y peridomésticos. Biomédica. 2011;31:264-8. http://dx.doi.org/10.7705/biomedica.v31i2.301
Salazar D, Calle J. Caracterización ecoepidemiológica de Rhodnius pallescens en la palma Attalea butyracea en la región momposina (Colombia). Actual Biol. 2003;25:31-8.
Jaramillo N, Schofield CJ, Gorla D, Caro-Riaño H, Moreno JE, Dujardin JP. The role of Rhodnius pallescens as a vector of Chagas disease in Colombia and Panamá. Res Rev Parasitol. 2000;60:75-82.
Aponte JD. Una revisión de la biología del Didelphis marsupialis y su relación con el mal de Chagas y la leishmaniasis. Hipótesis. 2013;96-101. Fecha de consulta: 20 de marzo de 2016. Disponible en: http://hipotesis.uniandes.edu.co/hipotesis/images/stories/edesp2013pdf/Una%20revision%20de%20la%20biologia%20del.pdf
Cantillo O, Chaverra D, Marcet P, Arboleda S, Triana O. Trypanosoma cruzi transmission in a Colombian Caribbean region suggests that secondary vectors play an important epidemiological role. Parasit Vectors. 2014;7:381-90. http://dx.doi.org/10.1186/1756-3305-7-381
Corporación Autónoma de la Meseta de Bucaramanga. Acuerdo del Consejo Directivo No1246, Bucaramanga, Santander, Colombia. 31 de mayo de 2013. Fecha de consulta: 15 de agosto de 2015. Disponible en: http://acmineria.com.co/sites/default/files/regulations/Acuerdo%20CDMB%201246%20de%202013%20-%20DMI-SINAP_0.pdf
Alcaldía Municipal de Bucaramanga, Santander. Santander 2030. Diagnóstico dimensión biofísico ambiental territorial de Santander. Fecha de consulta: 15 de agosto de 2015. Disponible en: https://www.uis.edu.co/webUIS/es/investigacionExtension/documentos/docInteres/Tomo%20I%20Dimension%20Biofisica%20Ambiental.pdf
Noireau F, Flores R, Vargas F. Trapping sylvatic Triatominae (Reduviidae) in hollow trees. Trans R Soc Trop Med Hyg. 1999;93:13-4.
Rojas MA. Nuevas estrategias de vigilancia entomológica para el control vectorial de la enfermedad de Chagas. En: Guhl F, editor. Primer Taller Internacional sobre Control de la Enfermedad de Chagas. Bogotá D.C.: Universidad de los Andes; 2005. p. 60-8.
Guerenstein PG, Guerin PM. Olfactory and behavioural responses of the blood-sucking bug Triatoma infestans to odours of vertebrate hosts. J Exp Biol. 2001;204:585-97.
Castro CM, Barret T, Santos W, Abad F, Rafael J. Attraction of Chagas disease vectors (Triatominae) to artificial light sources in the canopy of primary Amazon rainforest. Mem Inst Oswaldo Cruz. 2010;105:1061-4. http://dx.doi.org/10.1590/S0074-02762010000800019
Miller S, Dykes D, Polesky H. A simple salting out procedure for extracting DNA from human nucleated cells. Nucleic Acids Res. 1988;16:1215. http://dx.doi.org/10.1093/nar/16.3.1215
Moser D, Kirchhoff L, Donelson J. Detection of Trypanosoma cruzi by DNA amplification using the polymerase chain reaction. J. Clin Microbiol. 1989;27:1477-82.
Benítez JA, Araújo B, Contreras K, Rivas M, Ramírez P, Guerra W, et al. Urban outbreak of acute orally acquired Chagas disease in Táchira, Venezuela. J Infect Dev Ctries. 2013;7:638-41.
Walter A. Human activities and American trypanosomiasis. Review of the literature. Parasite.2003;10:191-204.
Soto H, Tibaduiza T, Montilla M, Triana O, Suárez DC, Torres M, et al. Investigación de vectores y reservorios en brote de Chagas agudo por posible transmisión oral en Aguachica, Cesar, Colombia. Cad Saúde Pública. 2014;30:746-56. http://dx.doi.org/10.1590/0102-311X00024013
Vásquez AM, Samudio FE, Saldaña A, Paz HM, Calzada JE. Eco-epidemiological aspects of Trypanosoma cruzi, Trypanosoma rangeli and their vector (Rhodnius pallescens) in Panamá. Rev Inst Med Trop Sao Paulo. 2004;46:217-22. http://dx.doi.org/10.1590/S0036-46652004000400008
Reyes-Lugo M. Bioecología de Panstrongyus geniculatus, vector de la enfermedad de Chagas en el centro-norte de Venezuela. Tribuna del Investigador. 2010;11:30-1.
Zeledón R. A new entomological indicator useful in epidemiological studies and in control campaigns against Chagas disease. Entomol Vect. 2003;10:269-76.
Angulo VM, Esteban L, Luna KP. Attalea butyracea próximas a las viviendas como posible fuente de infestación domiciliaria por Rhodnius prolixus (Hemiptera: Reduviidae) en los Llanos Orientales de Colombia. Biomédica. 2012;32:277-85. http://dx.doi.org/10.7705/biomedica.v32i2.430
Angulo VM, Esteban L, Urbano P, Hincapié E, Núñez LA. Comparación de métodos para la captura de triatominos (Hemiptera: Reduviidae) en palmas Attalea butyracea en los Llanos Orientales de Colombia. Biomédica. 2013;33:653-9. http://dx.doi.org/10.7705/biomedica.v33i4.835
Waleckx E, Gourbière S, Dumonteil E.Intrusive versus domiciliated triatomines and the challenge of adapting vector control practices against Chagas disease. Mem Inst Oswaldo Cruz. 2015;110:324-38. http://dx.doi.org/10.1590/0074-02760140409
Angulo VM, Castellanos YZ, Flórez M, Esteban L, Pérez W, Farfán AE, et al. Human Trypanosomiasis in the Eastern Plains of Colombia: New transmission scenario. Am J Trop Med Hyg. 2016;94:348-51. http://dx.doi.org/10.4269/ajtmh.15-0406
Some similar items:
- Omar Cantillo-Barraza, Andrés Gómez-Palacio, Diego Salazar, Ana María Mejía-Jaramillo, Jaime Calle, Omar Triana, Distribution and ecoepidemiology of the triatomine fauna (Hemiptera: Reduviidae) in Margarita Island, Bolívar, Colombia , Biomedica: Vol. 30 No. 3 (2010)
- Luis Reinel Vásquez, Cleber Galvão, Néstor A. Pinto, Humberto Granados, First report of Triatoma nigromaculata (Stål, 1859) (Hemiptera, Reduviidae, Triatominae) for Colombia. , Biomedica: Vol. 25 No. 3 (2005)
- Juan Fernando Ríos, Margarita Arboleda, Alba Nelly Montoya, Erika Patricia Alarcón, Gabriel Jaime Parra-Henao, Probable outbreak of oral transmission of Chagas disease in Turbo, Antioquia , Biomedica: Vol. 31 No. 2 (2011)
- Jaime Badel-Mogollón, Laura Rodríguez-Figueroa, Gabriel Parra-Henao, Spatio-temporal analysis of the biophysical and ecological conditions of Triatoma dimidiata (Hemiptera: Reduviidae: Triatominae) in the northeast region of Colombia , Biomedica: Vol. 37 No. Sup. 2 (2017): Suplemento 2, Entomología médica, 2017
- Andrea Arévalo, Julio César Carranza, Felipe Guhl, Gustavo Adolfo Vallejo, Electrophoretic patterns of salivary hemeproteins (nitrophorines) of Rhodnius colombiensis and R. prolixus (Hemiptera, Reduviidae, Triatominae) , Biomedica: Vol. 27 No. 1esp (2007): Enfermedad de Chagas
- Lyda Esteban, José Mauricio Montes, Víctor Manuel Angulo, Diversity of Triatominae (Hemiptera: Reduviidae) in Santander, Colombia: Epidemiological implications , Biomedica: Vol. 37 No. 1 (2017)
- Víctor Manuel Angulo, Lyda Esteban, Katherine Paola Luna, Attalea butyracea palms adjacent to housing as a source of infestation by Rhodnius prolixus (Hemiptera: Reduviidae) , Biomedica: Vol. 32 No. 2 (2012)
- Corina María Arroyo, Lyda Esteban, Silvia Catalá, Víctor Manuel Angulo, Antennal phenotype variation in sylvatic, peridomestic and domestic populations of Triatoma dimidiata (Hemiptera: Reduviidae) from Santander, Colombia. , Biomedica: Vol. 27 No. 1esp (2007): Enfermedad de Chagas
- Marlene Reyes, Víctor Manuel Angulo, Life cycle of Triatoma dimidiata Latreille, 1811 (Hemiptera, Reduviidae) under laboratory conditions: production of nymphs for biological tests , Biomedica: Vol. 29 No. 1 (2009)
- Paola Andrea Rueda , Sara Orozco , Juan Raúl Castro , Ángela María Londoño, Elsa María Vásquez, Andrea Arango, Carlos Esteban Builes , Incidence and prevalence of vitiligo by gender and age in the Colombian population , Biomedica: Vol. 45 No. 4 (2025)
| Article metrics | |
|---|---|
| Abstract views | |
| Galley vies | |
| PDF Views | |
| HTML views | |
| Other views | |