Modelado espacial de las infecciones por helmintos transmitidos por el suelo en Colombia en caso de cambio climático
Resumen
Introducción. Las geohelmintiasis siguen siendo una carga importante para la salud pública en Colombia, especialmente en zonas rurales y tropicales. Se espera que el cambio climático modifique las condiciones ambientales que favorecen la supervivencia y la transmisión de Ascaris lumbricoides, Trichuris trichiura y uncinarias.
Objetivo. Estimar la distribución espacial actual de estas infecciones y proyectar cambios en la prevalencia hacia 2035 con el cambio climático, con intervenciones en salud pública y sin ellas.
Materiales y métodos. Se realizó un estudio ecológico con modelado espacial que integró datos epidemiológicos, climáticos y biológicos. La prevalencia basal provino de la Encuesta Nacional de Parasitismo Intestinal (2012-2014). Se utilizaron proyecciones climáticas del producto satelital ERA5-Land (2024-2035) y modelos aditivos generalizados para estimar la idoneidad ambiental. Se establecieron rangos óptimos de temperatura y humedad mediante una revisión sistemática. Se modelaron dos escenarios: sin intervención y con desparasitación masiva y mejoras en saneamiento.
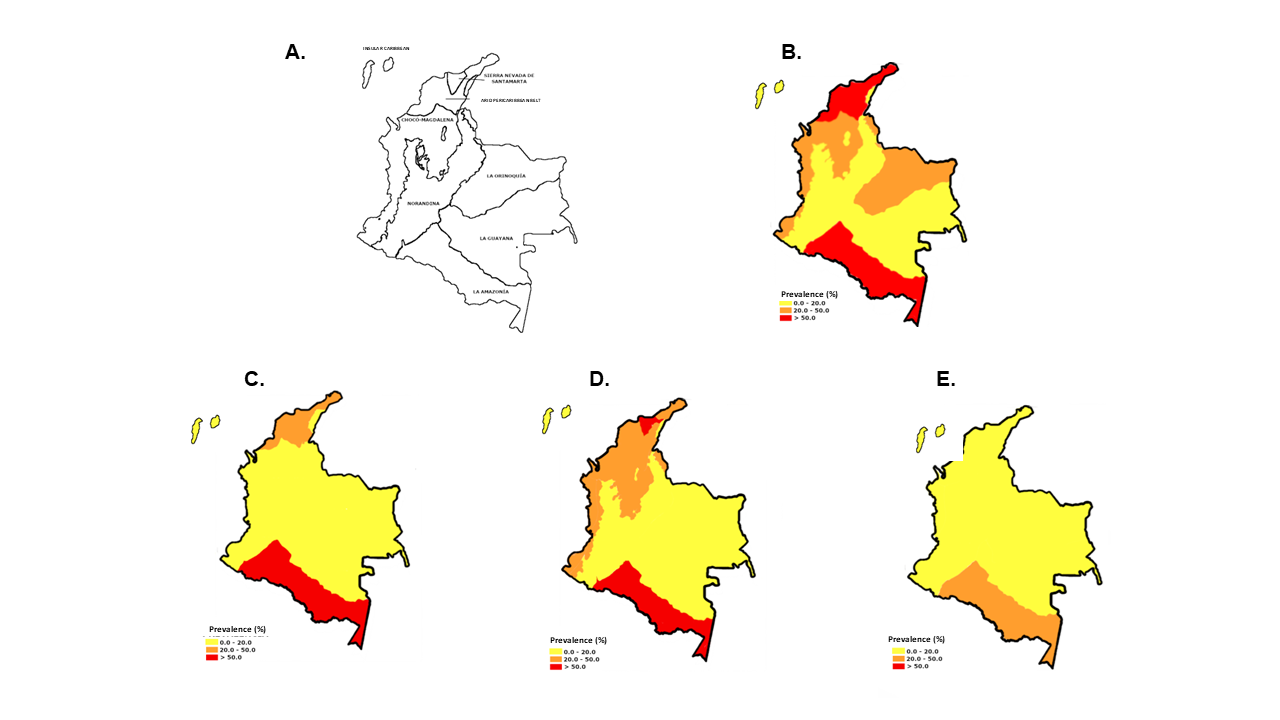
Resultados. La prevalencia basal fue de 11,3 % para A. lumbricoides, 18,4 % para T. trichiura y 6,4 % para uncinarias, con tasas más altas en la Amazonía y la Sierra Nevada de Santa Marta. Sin intervención, las prevalencias proyectadas aumentaron a 13,6, 21,2 y 8,0 %, respectivamente. Con intervención, se redujeron a 6,8, 12,7 y 5,6 %. La temperatura y humedad fueron predictores positivos significativos (p < 0,01), mientras que la altitud y la cobertura boscosa mostraron asociaciones negativas.
Conclusiones. El cambio climático podría intensificar la transmisión de las geohelmintiasis en Colombia hacia el 2035, pero las estrategias sostenidas de control pueden mitigar este impacto. El modelado espacial es una herramienta útil para planificar intervenciones focalizadas en salud pública.
Descargas
Referencias bibliográficas
World Health Organization. Soil-transmitted helminth infections. Accessed: July 30, 2025. Available at: https://www.who.int/news-room/fact-sheets/detail/soil-transmitted-helminthinfections
Jourdan PM, Lamberton PHL, Fenwick A, Addiss DG. Soil-transmitted helminth infections. Lancet. 2018;391:252-65. https://doi.org/10.1016/S0140-6736(17)31930-X
Clarke NE, Clements AC, Doi SA, Wang D, Campbell SJ, Gray D, et al. Differential effect of mass deworming and targeted deworming for soil-transmitted helminth control in children: A systematic review and meta-analysis. Lancet. 2017;389:287-97. https://doi.org/10.1016/S0140-6736(16)32123-7
World Health Organization. Preventive chemotherapy in human helminthiasis. Coordinated use of anthelminthic drugs in control interventions: a manual for health professionals and programme managers. Geneva: World Health Organization; 2006. p. 1-62.
Ministerio de Salud y Protección Social, Universidad de Antioquia. Encuesta Nacional de Parasitismo intestinal en Población Escolar 2012-2014. Medellín: Universidad de Antioquia, Ministerio de Salud y Protección Social; 2015. p. 1-173.
Pazmiño FA, Mora-Salamanca AF, Mahecha BSP, Moreno EJP, Olivera MJ, Ospina AK, et al. Prevalence of intestinal parasitism in preschool and school children in Colombia: Systematic review and meta-analysis. Trop Med Int Health. 2022;27:781-94. https://doi.org/10.1111/tmi.13800
Botero D, Restrepo M. Parasitosis humanas. 5a edición. Medellín: Corporación para Investigaciones Biológica; 2012. p. 1-723.
Vanalli C, Mari L, Casagrandi R, Gatto M, Cattadori IM. Helminth ecological requirements shape the impact of climate change on the hazard of infection. Ecol Lett. 2024;27:e14386. https://doi.org/10.1111/ele.14386
Booth M. Climate change and the neglected tropical diseases. Adv Parasitol. 2018;100:39-126. https://doi.org/10.1016/bs.apar.2018.02.001
Chen J, Gong Y, Chen Q, Li S, Zhou Y. Global burden of soil-transmitted helminth infections, 1990-2021. Infect Dis Poverty. 2024;13:77. https://doi.org/10.1186/s40249-024-01238-9
Tidman R, Abela-Ridder B, de Castañeda RR. The impact of climate change on neglected tropical diseases: A systematic review. Trans R Soc Trop Med Hyg. 2021;115:147-68. https://doi.org/10.1093/trstmh/traa192
Schuele SA, Clowes P, Kowuor DO, Nsojo A, Mangu C, Riess H, et al. Ascaris lumbricoides infection and its relation to environmental factors in the Mbeya region of Tanzania, a crosssectional, population-based study. PLoS ONE. 2014;9:e92032. https://doi.org/10.1371/journal.pone.0092032
Kim M, Pyo K, Hwang Y, Park kh, Hwang IG, Chai JY, et al. Effect of temperature on embryonation of Ascaris suum eggs in an environmental chamber. Korean J Parasitol. 2012;50:239-42. https://doi.org/10.3347/kjp.2012.50.3.239
Chammartin F, Guimarães LH, Scholte RG, Bavia ME, Utzinger J, Vounatsou P. Spatiotemporal distribution of soil-transmitted helminth infections in Brazil. Parasit Vectors. 2014;18:440. https://doi.org/10.1186/1756-3305-7-440
Huang SY, Lai YS, Fang YY. The spatial-temporal distribution of soil-transmitted helminth infections in Guangdong Province, China: A geostatistical analysis of data derived from the three national parasitic surveys. PLoS Negl Trop Dis. 2022;16:e0010622. https://doi.org/10.1371/journal.pntd.0010622
Hernández J, Hurtado A, Ortiz R, Walschburger T. Unidades biogeográficas de Colombia. En la diversidad biológica de Iberoamérica. 1a edición. Xalapa: Acta Zoológica Mexicana; 1992. p. 95-135.
Mitra AK, Mawson AR. Neglected tropical diseases: Epidemiology and global burden. Trop Med Infect Dis. 2017;2:36. https://doi.org/10.3390/tropicalmed2030036
Carlson CJ, Albery GF, Merow C, Trisos CH, Zipfel CM, Eskew EA, et al. Climate change increases cross-species viral transmission risk. Nature. 2022;607:555-62. https://doi.org/10.1038/s41586-022-04788-w
Caminade C, McIntyre KM, Jones AE. Impact of recent and future climate change on vectorborne diseases. Ann NY Acad Sci. 2019;1436:157-73. https://doi.org/10.1111/nyas.13950
Rocklöv J, Dubrow R. Climate change: An enduring challenge for vector-borne disease prevention and control. Nat Immunol. 2020;21:479-83. https://doi.org/10.1038/s41590-020-0648-y
Saboyá M, Catalá L, Ault S, Nicholls R. Prevalence and intensity of infection of soil-transmitted helminths in Latin America and the Caribbean countries: Mapping at second administrative level 2000-2010. Washington, D.C: Pan American Health Organization; 2011. p. 1-106.
Candela E, Goizueta C, Sandon L, Muñoz-Antoli C, Periago MV. The relationship between soil-transmitted helminth infections and environmental factors in Puerto Iguazú, Argentina: Cross-sectional study. JMIR Public Health Surveill. 2023;9:e41568. https://doi.org/10.2196/41568
Maddren R, Phillips A, Ower A, Landeryou T, Mengistu B, Anjulo U, et al. Soil-transmitted helminths and schistosome infections in Ethiopia: A systematic review of progress in their control over the past 20 years. Parasit Vectors. 2023;16:203. https://doi.org/10.1186/s13071-023-05815-z
Sartorius B, Cano J, Simpson H, Tusting LS, Marczak LB, Miller-Petrie MK, et al. Prevalence and intensity of soil-transmitted helminth infections of children in sub-Saharan Africa, 2000-18: A geospatial analysis. Lancet Glob Health. 2021;9:e52-e60. https://doi.org/10.1016/S2214-109X(20)30398-3
Newbold LK, Burthe SJ, Oliver AE, Gweon HS, Barnes CJ, Daunt F, et al. Helminth burden and ecological factors associated with alterations in wild host gastrointestinal microbiota. ISME J. 2017;11:663-75. https://doi.org/10.1038/ismej.2016.153
Hall A, Holland C. Geographical variation in Ascaris lumbricoides fecundity and implications for helminth control. Parasitol Today. 2000;16:540-4. https://doi.org/10.1016/s0169-4758(00)01779-8
Ali A, Niaz S, Nasreen N, Khan A, Shafeeq S, Aguilar-Marcelino L, et al. Temporal and spatial patterns of Trichuris trichiura eggs: A potential threat to human health in Pakistan. Helminthologia. 2024;61:11-9. https://doi.org/10.2478/helm-2024-0009
Pullan RL, Kabatereine NB, Quinnell RJ, Brooker S. Spatial and genetic epidemiology of hookworm in a rural community in Uganda. PLoS Negl Trop Dis. 2010;4:e713. https://doi.org/10.1371/journal.pntd.0000713
Chammartin F, Scholte RG, Malone JB, Bavia ME, Nieto P, Utzinger J, et al. Modelling the geographical distribution of soil-transmitted helminth infections in Bolivia. Parasit Vectors. 2013;6:152. https://doi.org/10.1186/1756-3305-6-152
Weatherhead JE, Hotez PJ. Worm infections in children. Pediatr Rev. 2015;36:341-52. https://doi.org/10.1542/pir.36-8-341
Kim MK, Pyo KH, Hwang YS, Park KH, Hwang IG, Chai JY, et al. Effect of temperatura on embryonation of Ascaris suum eggs in an environmental chamber. Korean J Parasitol. 2012;50:239-42. https://doi.org/10.3347/kjp.2012.50.3.239
Weaver HJ, Hawdon JM, Hoberg EP. Soil-transmitted helminthiases: Implications of climate change and human behaviour. Trends Parasitol. 2010;26:574-81. https://doi.org/10.1016/j.pt.2010.06.009
Bethony J, Brooker S, Albonico M, Geiger SM, Loukas A, Diemert D, et al. Soil-transmitted helminth infections: ascariasis, trichiuriasis, and hookworm. Lancet. 2006;367:1521-32. https://doi.org/10.1016/S0140-6736(06)68653-4
Kaliappan S, Ramanujam K, Manuel M, Farzana J, Janagaraj V, Laxmanan S, et al. Soiltransmitted helminth infections after mass drug administration for lymphatic filariasis in rural southern India. Trop Med Int Health. 2022;27:81-91 https://doi.org/10.1111/tmi.13697
Servián A, Garimano N, Santini MS. Systematic review and meta-analysis of soil-transmitted helminth infections in South America (2000-2024). Acta Trop. 2024;260:107400. https://doi.org/10.1016/j.actatropica.2024.107400
Savioli L, Albonico M, Engels D, Montresor A. Progress in the prevention and control of schistosomiasis and soil-transmitted helminthiasis. Parasitol Int. 2004;53:103-13. https://doi.org/10.1016/j.parint.2004.01.001
Algunos artículos similares:
- Óscar René Sorto, Alexandra Manoella Portillo, Miguel Ángel Aragón, Martha IdalÍ Saboyá, María Paz Ade, Miguel Ángel Minero, Marta Alicia Hernández, Amada Gloria Mena, Rodolfo Peña, Victor Manuel Mejía, Keith Carter, Prevalencia e intensidad de la infección por geohelmintos y prevalencia de la malaria en escolares de El Salvador , Biomédica: Vol. 35 Núm. 3 (2015)
- Luis Caraballo, Josefina Zakzuk, Consideraciones sobre la evolución de la respuesta inmunitaria Th2 y sus posibles relaciones con parasitosis y alergia , Biomédica: Vol. 32 Núm. 1 (2012)
Derechos de autor 2025 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |
Datos de los fondos

























