Estandarización de zimosán opsonizado como estímulo en la técnica de la 1,2,3-dihidrorrodamina para evaluar el estallido respiratorio del neutrófilo
Resumen
Introducción. La enfermedad granulomatosa crónica es un defecto de la fagocitosis por deficiencia de gp91phox, p22phox, p47phox, p40phox y p67phox (forma clásica). Recientemente, se describió la deficiencia de EROS y p40phox como responsables de la forma no clásica. La técnica de oxidación de la 1,2,3-dihidrorrodamina –usando como estímulo el forbol-12-miristato-13-acetato– se utiliza para el diagnóstico de la enfermedad granulomatosa crónica clásica. Sin embargo, para la detección de la oxidación mediada por EROS y p40phox, se requiere de otros estímulos como zimosán, Escherichia coli o Staphylococcus aureus.
Objetivo. Estandarizar el estímulo con zimosán en la técnica de la 1,2,3-dihidrorrodamina para evaluar el estallido respiratorio del neutrófilo.
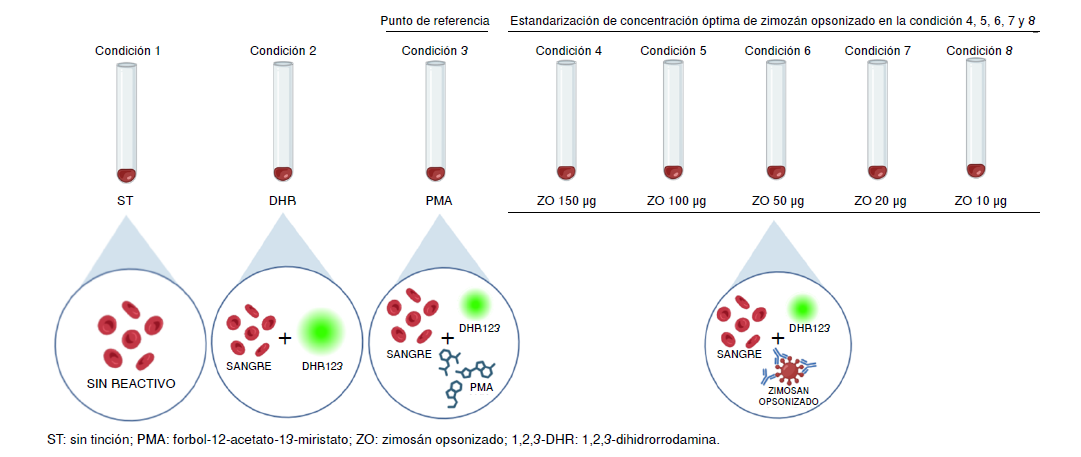
Materiales y métodos. Se obtuvo sangre de cinco sujetos sanos previo consentimiento informado. Se utilizó la técnica de 1,2,3-dihidrorrodamina usando el forbol-12-miristato-13-acetato como control y diferentes cantidades de zimosán opsonizado (150, 100, 50, 20 y 10 μg). Por citometría de flujo, se obtuvo la intensidad de fluorescencia media de la rodamina 1,2,3 en las poblaciones de neutrófilos y se calculó el índice de oxidación. Se utilizaron las pruebas de Kolmogorov-Smirnov, ANOVA y el análisis post-hoc de Tukey. Se consideró un valor de p ≤ 0,05 como estadísticamente significativo.
Resultados. El forbol-12-miristato-13-acetato incrementó la intensidad de la fluorescencia media de la rodamina 1,2,3 en los sujetos sanos. Entre las diferentes condiciones de zimosán probadas, la de 50 μg fue la cantidad óptima y reproducible en todos los controles por el análisis estadístico y los hallazgos citométricos.
Conclusiones. Se presenta la optimización de la técnica 1,2,3-dihidrorrodamina empleando el zimosán como estímulo.
Descargas
Referencias bibliográficas
Yu HH, Yang YH, Chiang BL. Chronic granulomatous disease: A comprehensive review. Clin Rev Allergy Immunol. 2021;61:101-13. https://doi.org/10.1007/s12016-020-08800-x
Randzavola LO, Mortimer PM, Garside E, Dufficy ER, Schejtman A, Roumelioti G, et al. EROS is a selective chaperone regulating the phagocyte NADPH oxidase and purinergic signalling. Elife. 2022;11. https://doi.org/10.7554/eLife.76387
López-Hernández I, Suárez-Gutiérrez M, Santos-Chávez EE, Espinosa S, Blancas-Galicia L. Chronic granulomatous disease. Update and review. Rev Alerg Mex. 2019;66:232-45. https://doi.org/10.29262/ram.v66i2.577
Dinauer MC. Inflammatory consequences of inherited disorders affecting neutrophil function. Blood. 2019;133:2130-9. https://doi.org/10.1182/blood-2018-11-844563
Matute JD, Arias AA, Wright NA, Wrobel I, Waterhouse CC, Li XJ, et al. A new genetic subgroup of chronic granulomatous disease with autosomal recessive mutations in p40phox and selective defects in neutrophil NADPH oxidase activity. Blood. 2009;114:3309-15. https://doi.org/10.1182/blood-2009-07-231498
van de Geer A, Nieto-Patlan A, Kuhns DB, Tool AT, Arias AA, Bouaziz M, et al. Inherited p40phox deficiency differs from classic chronic granulomatous disease. J Clin Invest. 2018;128:3957-75. https://doi.org/10.1172/JCI97116
Neehus AL, Fusaro M, consortium NCF, Levy R, Bustamante J. A new patient with p40phox deficiency and chronic immune thrombocytopenia. J Clin Immunol. 2023;43:1173-7. https://doi.org/10.1007/s10875-023-01498-4
Arnadottir GA, Norddahl GL, Gudmundsdottir S, Agustsdottir AB, Sigurdsson S, Jensson BO, et al. A homozygous loss-of-function mutation leading to CYBC1 deficiency causes chronic granulomatous disease. Nat Commun. 2018;9:4447. https://doi.org/10.1038/s41467-018-06964-x
Thomas DC, Charbonnier LM, Schejtman A, Aldhekri H, Coomber EL, Dufficy ER, et al. EROS/CYBC1 mutations: Decreased NADPH oxidase function and chronic granulomatous disease. J Allergy Clin Immunol. 2019;143:782-5.e1. https://doi.org/10.1016/j.jaci.2018.09.019
Wright M, Chandrakasan S, Okou DT, Yin H, Jurickova I, Denson LA, et al. Early onset granulomatous colitis associated with a mutation in NCF4 resolved with hematopoietic stem cell transplantation. J Pediatr. 2019;210:220-5. https://doi.org/10.1016/j.jpeds.2019.03.042
Chester AE, Kuhns D, Lau K, Holland S, Canfield S, Garcia C, et al. A rare cause of necrotizing pneumonia in an adult woman: p40phox (NCF4) deficient autosomal recessive Chronic Granulomatous Disease. Clin Immunol. 2023;250(Supl.). https://doi.org/10.1016/j.clim.2023.109525
Pérez-Heras I, Tsilifis C, Slatter MA, Brynjolfsson SF, Haraldsson A, Gennery AR. HSCT in two brothers with CGD arising from mutations in CYBC1 corrects the defect in neutrophil function. Clin Immunol. 2021;229:108799. https://doi.org/10.1016/j.clim.2021.108799
Chiriaco M, De Matteis A, Cifaldi C, Di Matteo G, Rivalta B, Passarelli C, et al. Characterization of AR-CGD female patient with a novel homozygous deletion in CYBC1 gene presenting with unusual clinical phenotype. Clin Immunol. 2023;251:109316. https://doi.org/10.1016/j.clim.2023.109316
Mortimer PM, Nichols E, Thomas J, Shanbhag R, Singh N, Coomber EL, et al. A novel mutation in EROS (CYBC1) causes chronic granulomatous disease. Clin Immunol. 2023;255:109761. https://doi.org/10.1016/j.clim.2023.109761
Roos D, de Boer M. Molecular diagnosis of chronic granulomatous disease. Clin Exp Immunol. 2014;175:139-49. https://doi.org/10.1111/cei.12202
Nauseef WM. How human neutrophils kill and degrade microbes: An integrated view. Immunol Rev. 2007;219:88-102. https://doi.org/10.1111/j.1600-065X.2007.00550.x
Askarian F, Wagner T, Johannessen M, Nizet V. Staphylococcus aureus modulation of innate immune responses through Toll-like (TLR), (NOD)-like (NLR) and C-type lectin (CLR) receptors. FEMS Microbiol Rev. 2018;42:656-71. https://doi.org/10.1093/femsre/fuy025
Makni-Maalej K, Chiandotto M, Hurtado-Nedelec M, Bedouhene S, Gougerot-Pocidalo MA, Dang PM, et al. Zymosan induces NADPH oxidase activation in human neutrophils by inducing the phosphorylation of p47phox and the activation of Rac2: involvement of protein tyrosine kinases, PI3Kinase, PKC, ERK1/2 and p38MAPkinase. Biochem Pharmacol. 2013;85:92-100. https://doi.org/10.1016/j.bcp.2012.10.010
Belambri SA, Rolas L, Raad H, Hurtado-Nedelec M, Dang PM, El-Benna J. NADPH oxidase activation in neutrophils: Role of the phosphorylation of its subunits. Eur J Clin Invest. 2018;48(Suppl.2):e12951. https://doi.org/10.1111/eci.12951
Schmidlin M, Alt M, Vogel G, Voegeli U, Brodmann P, Bagutti C. Contaminations of laboratory surfaces with Staphylococcus aureus are affected by the carrier status of laboratory staff. J Appl Microbiol. 2010;109:1284-93. https://doi.org/10.1111/j.1365-2672.2010.04749.x
Bereswill S, Fischer A, Dunay IR, Kuhl AA, Gobel UB, Liesenfeld O, et al. Pro-inflammatory potential of Escherichia coli strains K12 and Nissle 1917 in a murine model of acute ileitis. Eur J Microbiol Immunol (Bp). 2013;3:126-34. https://doi.org/10.1556/EuJMI.3.2013.2.6
Hirt W, Nebe T, Birr C. Phagotest and Bursttest (Phagoburst), test kits for study of phagocyte functions. Wien Klin Wochenschr. 1994;106:250-2.
Rodríguez-Santiago B, Armengol L. Tecnologías de secuenciación de nueva generación en diagnóstico genético pre- y postnatal. Diagn Prenat. 2012;23:56-66. https://doi.org/10.1016/j.diapre.2012.02.001
Derechos de autor 2024 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























