Actualización sobre la resistencia antimicrobiana en instituciones de salud de nivel III y IV en Colombia entre enero del 2018 y diciembre del 2021
Resumen
Introducción. El comportamiento de la resistencia antimicrobiana es fundamental en el mejoramiento y ajuste de los programas de optimización de uso de antimicrobianos, la implementación de las guías terapéuticas y las precauciones que limitan la transmisión cruzada de bacterias resistentes entre pacientes. Desde el inicio del 2020, la pandemia del SARS-CoV-2 desafió profundamente al sistema de salud y, según algunos reportes, aumentó las tasas de resistencia antimicrobiana.
Objetivo. Describir el comportamiento de la resistencia antimicrobiana en los microrganismos más frecuentes en veinte hospitales colombianos durante el periodo 2018-2021.
Materiales y métodos. Se trata de un estudio descriptivo basado en la información microbiológica reportada por veinte instituciones de salud de nivel III y IV, entre enero de 2018 y diciembre de 2021, en doce ciudades de Colombia, las cuales hacen parte del “Grupo para el estudio de la resistencia nosocomial en Colombia”, liderado por la Universidad El Bosque. La identificación de género y especie de los microorganismos más frecuentes, junto con su perfil de resistencia frente a antibióticos marcadores, se determinaron mediante el análisis de los datos vía WHONET.
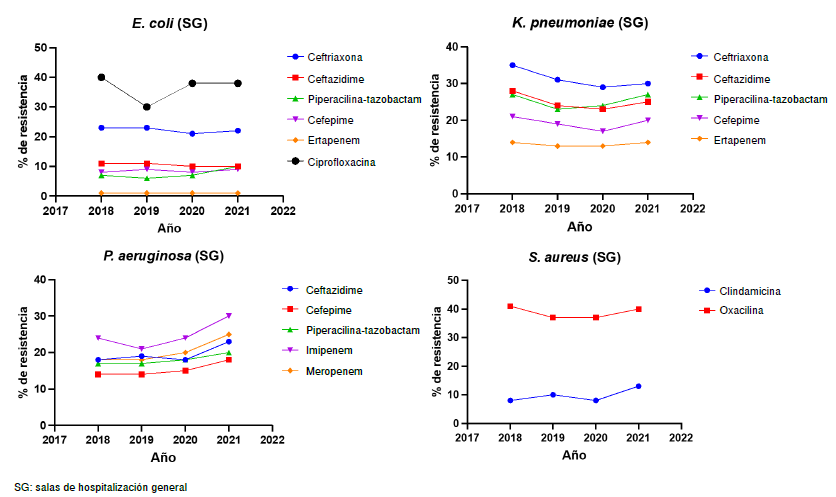
Resultados. En general, los 10 microorganismos más frecuentes analizados a lo largo de los 4 años no presentaron cambios estadísticamente significativos en sus perfiles de resistencia durante los cuatro años del periodo evaluado, de 2018 a 2021. En contraste, Pseudomonas aeruginosa aumentó su resistencia frente a piperacilina-tazobactam y carbapenémicos, lo cual fue estadísticamente significativo.
Conclusiones. Los cambios en la resistencia antimicrobiana en estos años no han sido estadísticamente significativos, excepto para P. aeruginosa, bacteria que mostró un incremento en las tasas de resistencia a piperacilina-tazobactam y carbapenémicos.
Descargas
Referencias bibliográficas
Haustein T, Gastmeier P, Holmes A, Lucet JC, Shannon RP, Pittet D, et al. Use of benchmarking and public reporting for infection control in four high-income countries. Lancet Infect Dis. 2011;11:471-81. https://doi.org/10.1016/S1473-3099(10)70315-7
World Health Organization. Guidelines for the prevention and control of carbapenemresistant Enterobacteriaceae, Acinetobacter baumannii and Pseudomonas aeruginosa in health care facilities. Geneva: World Health Organization; 2017.
Lan P, Jiang Y, Zhou J, Yu Y. A global perspective on the convergence of hypervirulence and carbapenem resistance in Klebsiella pneumoniae. J Glob Antimicrob Resist. 2021;25:26-34. https://doi.org/10.1016/j.jgar.2021.02.020
Critchley IA, Karlowsky JA. Optimal use of antibiotic resistance surveillance systems. Clin Microbiol Infect. 2004;10:502-11. https://doi.org/10.1111/j.1469-0691.2004.00911.x
Harbarth S, Balkhy HH, Goossens H, Jarlier V, Kluytmans J, Laxminarayan R, et al. Antimicrobial resistance: One world, one fight! Antimicrob Resist Infect Control. 2015;4:1-15. https://doi.org/10.1186/s13756-015-0091-2
Castanheira M, Deshpande LM, Mendes RE, Canton R, Sader HS, Jones RN. Variations in the occurrence of resistance phenotypes and carbapenemase genes among Enterobacteriaceae isolates in 20 years of the SENTRY antimicrobial surveillance program. Open Forum Infect Dis. 2019;6(Suppl.1):S23-33. https://doi.org/10.1093/ofid/ofy347
Paterson DL, Rossi F, Baquero F, Hsueh PR, Woods GL, Satishchandran V, et al. In vitro susceptibilities of aerobic and facultative Gram-negative bacilli isolated from patients with intra-abdominal infections worldwide: The 2003 Study for Monitoring Antimicrobial Resistance Trends (SMART). Int J Antimicrob Agents. 2005;55:965-73. https://doi.org/10.1093/jac/dki117
Canton R, Gijon D, Ruiz-Garbajosa P. Antimicrobial resistance in ICUs: An update in the light of the COVID-19 pandemic. Curr Opin Crit Care. 2020;26:433-41. https://doi.org/10.1097/MCC.0000000000000755
Shortridge D, Gales AC, Streit JM, Huband MD, Tsakris A, Jones RN. Geographic and temporal patterns of antimicrobial resistance in pseudomonas aeruginosa over 20 years from the SENTRY Antimicrobial Surveillance Program, 1997-2016. Open Forum Infect Dis. 2019;6(Suppl.1):S63-8. https://doi.org/10.1093/ofid/ofy343
Segala FV, Bavaro DF, Di Gennaro F, Salvati F, Marotta C, Saracino A, et al. Impact of sars-cov-2 epidemic on antimicrobial resistance: A literature review. Viruses. 2021;13:1-15. https://doi.org/10.3390/v13112110
Jeon K, Jeong S, Lee N, Park MJ, Song W, Kim HS, et al. Impact of COVID-19 on antimicrobial consumption and spread of multidrug-resistance in bacterial infections. Antibiotics. 2022;11:1-12. https://doi.org/10.3390/antibiotics11040535
Kariyawasam RM, Julien DA, Jelinski DC, Larose SL, Rennert-May E, Conly JM, et al. Antimicrobial resistance (AMR) in COVID-19 patients: A systematic review and metaanalysis (November 2019–June 2021). Antimicrob Resist Infect Control. 2022;11. https://doi.org/10.1186/s13756-022-01085-z
Hughes S, Troise O, Donaldson H, Mughal N, Moore LSP. Bacterial and fungal coinfection among hospitalised patients with COVID-19. Clin Microbiol Infect. 2020;26:1395-9. https://doi.org/10.1016/j.cmi.2020.06.025
van Duin D, Barlow G, Nathwani D. The impact of the COVID-19 pandemic on antimicrobial resistance: A debate. JAC Antimicrob Resist. 2020;2:4-5. https://doi.org/10.1093/jacamr/dlaa053
Bork JT, Leekha S, Claeys K, Seung H, Tripoli M, Amoroso A, et al. Change in hospital antibiotic use and acquisition of multidrug-resistant gram-negative organisms after the onset of coronavirus disease 2019. Infect Control Hosp Epidemiol. 2021;42:1115-7. https://doi.org/10.1017/ice.2020.1360
Russo A, Gavaruzzi F, Ceccarelli G, Borrazzo C, Oliva A, Alessandri F, et al. Multidrugresistant Acinetobacter baumannii infections in COVID-19 patients hospitalized in intensive care unit. Infection. 2022;50:83-92. https://doi.org/10.1007/s15010-021-01643-4
Khojasteh S, Jafarzdeh J, Hosseini SA, Haghani I, Turki H, Aghaei Gharehbolagh S, et al. Candida auris and COVID-19: A health threatening combination. Curr Med Mycol. 2022;8:44-50. https://doi.org/10.18502/cmm.8.3.11211
Patel A, Emerick M, Cabunoc MK, Williams MH, Preas MA, Schrank G, et al. Rapid spread and control of multidrug-resistant Gram-negative bacteria in COVID-19 patient care units. Emerg Infect Dis. 2021;27:1234-7. https://doi.org/10.3201/eid2704.204036
Stelling JM, O’Brien TF. Surveillance of antimicrobial resistance: The WHONET program. Clin Infect Dis. 1997;24(Suppl.1):S157-68. https://doi.org/10.1093/clinids/24.supplement_1.s157
Clinical and Laboratory Standards Institute (CLSI). Performance standards for antimicrobial susceptibility testing. 32nd edition. Wayne, PA: Clinical and Laboratory Standards Institute; 2022.
Clinical and Laboratory Standards Institute (CLSI). Analysis and presentation of cumulative antimicrobial susceptibility test data; Approved guideline –Fourth edition. CLSI document M39-A4. Wayne, PA: Clinical and Laboratory Standards Institute; 2014.
Plante JA, Mitchell BM, Plante KS, Debbink K, Weaver SC, Menachery VD. The variant gambit: COVID-19’s next move. Cell Host Microbe. 2021;29:508-15. https://doi.org/10.1016/j.chom.2021.02.020
Ovalle MV, Saavedra SY, González MN, Hidalgo AM, Duarte C, Beltrán M. Resultados de la vigilancia nacional de la resistencia antimicrobiana de enterobacterias y bacilos Gram negativos no fermentadores en infecciones asociadas a la atención de salud, Colombia, 2012-2014. Biomédica. 2017;37:473-85. https://doi.org/10.7705/biomedica.v37i4.3432
Martínez-Guerra BA, González-Lara MF, de León-Cividanes NA, Tamez-Torres KM, Román-Montes CM, Rajme-López S, et al. Antimicrobial resistance patterns and antibiotic use during hospital conversion in the COVID-19 pandemic. Antibiotics. 2021;10:1-9. https://doi.org/10.3390/antibiotics10020182
Nowak MD, Sordillo EM, Gitman MR, Paniz Mondolfi AE. Coinfection in SARS-CoV-2 infected patients: Where are influenza virus and rhinovirus/enterovirus? J Med Virol. 2020;92:1699-700. https://doi.org/10.1002/jmv.25953
Maes M, Higginson E, Pereira-Dias J, Curran MD, Parmar S, Khokhar F, et al. Ventilatorassociated pneumonia in critically ill patients with COVID-19. Crit Care. 2021;25:1-11. https://doi.org/10.1186/s13054-021-03460-5
Briceño DF, Correa A, Valencia C, Torres JA, Pacheco R, Montealegre MC, et al. Antimicrobial resistance of Gram negative bacilli isolated from terciary-care hospitals in Colombia. Biomédica. 2010;30:371-81. https://doi.org/10.7705/biomedica.v30i3.271
Fournier PE, Richet H. The epidemiology and control of Acinetobacter baumannii in health care facilities. Clin Infect Dis. 2006;42:692-9. https://doi.org/10.1086/500202
Ovalle MV, Saavedra SY, Rodríguez MK. Informe de resultados de la vigilancia por laboratorio de resistencia antimicrobiana en infecciones asociadas a la atención en salud. Bogotá, D.C.: Instituto Nacional de Salud; 2018.
Ovalle MV, Duarte C, Zambrano C. Informe de resultados de la vigilancia por laboratorio de resistencia antimicrobiana en infecciones asociadas a la atención en salud. Bogotá, D.C.: Instituto Nacional de Salud; 2019.
Ovalle MV, Duarte C, Leal AL, Zambrano C. Informe de resultados de la vigilancia por laboratorio de resistencia antimicrobiana en infecciones asociadas a la atención en salud. Bogotá, D.C.: Instituto Nacional de Salud; 2020.
Ovalle MV, Duarte C, Flórez AC, Leal AL, Zambrano C. Informe de resultados de la vigilancia por laboratorio de resistencia antimicrobiana en infecciones asociadas a la atención en salud. Bogotá, D.C.: Instituto Nacional de Salud; 2021.
Organización Panamericana de la Salud. Reporte de situación COVID-19 Colombia No. 285- 25 de agosto 2022. Fecha de consulta: 20 de agosto del 2023. Disponible en: https://www.paho.org/es/reportes-situacion-covid-19-colombia
Saavedra Trujillo CH. Consenso colombiano de atención, diagnóstico y manejo de la infección por SARS-CoV-2/COVID-19 en establecimientos de atención de la salud. Recomendaciones basadas en consenso de expertos e informadas en la evidencia. Infectio. 2020;24:50-60. https://doi.org/10.22354/in.v24i3.889
Rawson TM, Ming D, Ahmad R, Moore LSP, Holmes AH. Antimicrobial use, drug-resistant infections and COVID-19. Nat Rev Microbiol. 2020;18:409-10. https://doi.org/10.1038/s41579-020-0395-y
Chen N, Zhou M, Dong X, Qu J, Gong F, Han Y, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: A descriptive study. Lancet. 2020;395:507-513. https://doi.org/10.1016/S0140-6736(20)30211-7
Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: A retrospective cohort study. Lancet. 2020;395:1054-62. https://doi.org/10.1016/S0140-6736(20)30566-3
Rawson TM, Moore LSP, Zhu N, Ranganathan N, Skolimowska K, Gilchrist M, et al. Bacterial and fungal coinfection in individuals with coronavirus: A rapid review to support COVID-19 antimicrobial prescribing. Clin Infect Dis. 2020;71:2459-68. https://doi.org/10.1093/cid/ciaa530
Rawson TM, Moore LSP, Castro-Sánchez E, Charani E, Davies F, Satta G, et al. COVID-19 and the potential long-term impact on antimicrobial resistance. J Antimicrob Chemother. 2020;75:1681-4. https://doi.org/10.1093/jac/dkaa194
Thomas GR, Corso A, Pasterán F, Shal J, Sosa A, Pillonetto M, et al. Increased detection of carbapenemase-producing Enterobacterales bacteria in Latin America and the Caribbean during the COVID-19 pandemic. Emerg Infect Dis. 2022;28:1-8. https://doi.org/10.3201/eid2811.220415
Algunos artículos similares:
- Elizabeth Borrero, Gabriel Carrasquilla, Neal Alexander, Descentralización y reforma: ¿cuál es su impacto sobre la incidencia de malaria en los municipios colombianos? , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Raúl Murillo, Ricardo Cendales, Carolina Wiesner, Marion Piñeros, Sandra Tovar, Efectividad de la citología cérvico-uterina para la detección temprana de cáncer de cuello uterino en el marco del sistema de salud de Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- Sandra Lorena Girón, Julio César Mateus, Fabián Méndez, Impacto de un botadero a cielo abierto en el desarrollo de síntomas respiratorios y en costos familiares de atención en salud de niños entre 1 y 5 años en Cali, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- José Joaquín Carvajal, Ligia Inés Moncada, Mauricio Humberto Rodríguez, Ligia del Pilar Pérez, Víctor Alberto Olano, Caracterización preliminar de los sitios de cría de Aedes (Stegomyia) albopictus (Skuse, 1894) (Diptera: Culicidae) en el municipio de Leticia, Amazonas, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- Andrés Páez, Gloria Rey, Carlos Agudelo, Alvaro Dulce, Edgar Parra, Hernando Díaz-Granados, Damaris Heredia, Luis Polo, Brote de rabia urbana transmitida por perros en el distrito de Santa Marta, Colombia, 2006-2008 , Biomédica: Vol. 29 Núm. 3 (2009)
- Patricia Escobar, Katherine Paola Luna, Indira Paola Hernández, César Mauricio Rueda, María Magdalena Zorro, Simon L. Croft, Susceptibilidad in vitro a hexadecilfosfocolina (miltefosina), nifurtimox y benznidazole de cepas de Trypanosoma cruzi aisladas en Santander, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- Gustavo Pradilla, Julio César Mantilla, Reynaldo Badillo, Encefalitis rábica humana por mordedura de murciélago en un área urbana de Colombia , Biomédica: Vol. 29 Núm. 2 (2009)
- Mauricio Beltrán, María Cristina Navas, María Patricia Arbeláez, Jorge Donado, Sergio Jaramillo, Fernando De la Hoz, Cecilia Estrada, Lucía del Pilar Cortés, Amalia de Maldonado, Gloria Rey, Seroprevalencia de infección por virus de la hepatitis B y por virus de la inmunodeficiencia humana en una población de pacientes con múltiples transfusiones en cuatro hospitales, Colombia, Sur América , Biomédica: Vol. 29 Núm. 2 (2009)
- Rosa Magdalena Uscátegui, Adriana M. Correa, Jaime Carmona-Fonseca, Cambios en las concentraciones de retinol, hemoglobina y ferritina en niños palúdicos colombianos , Biomédica: Vol. 29 Núm. 2 (2009)
- Claudia M.E. Romero-Vivas, Luis Eduardo Castro, Lila Visbal, Ana María Santos, Esther Díaz, Miasis cutánea por Cochliomyia hominivorax (Coquerel) (Díptera: Calliphoridae) en el Hospital Universidad del Norte, Soledad, Atlántico , Biomédica: Vol. 29 Núm. 1 (2009)
Derechos de autor 2023 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























