Caracterización molecular y fenotípica de aislamientos clínicos de Salmonella Typhimurium variante monofásica (1,4,[5],12:i:-) recuperados en Colombia
Resumen
Introducción. La variante monofásica (1,4,[5],12:i:-) de Salmonella Typhimurium ocupa los primeros lugares en los programas de vigilancia de Salmonella a nivel mundial. En Colombia, Salmonella enterica variante monofásica alcanza el cuarto lugar en cuanto a los aislamientos clínicos recuperados por medio de la vigilancia por laboratorio del Grupo de Microbiología del Instituto Nacional de Salud, pero se desconoce si dichos aislamientos están relacionados con la variante monofásica de Typhimurium que circula a nivel global, y con sus características genéticas y fenotípicas.
Objetivo. Caracterizar los aislamientos de Salmonella monofásica recuperados en Colombia entre el 2015 y el 2018 por el Grupo de Microbiología del Instituto Nacional de Salud.
Materiales y métodos. Se analizaron 286 aislamientos clínicos de Salmonella enterica variante monofásica mediante PCR o secuenciación del genoma completo (Whole Genome Sequencing, WGS) para confirmar si correspondían a Salmonella Typhimurium variante monofásica, en tanto que, en 54 aislamientos, se determinó la estructura genética del operón que codifica la segunda fase flagelar y, en 23, se evaluó la motilidad, el crecimiento y la expresión de las proteínas de membrana externa.
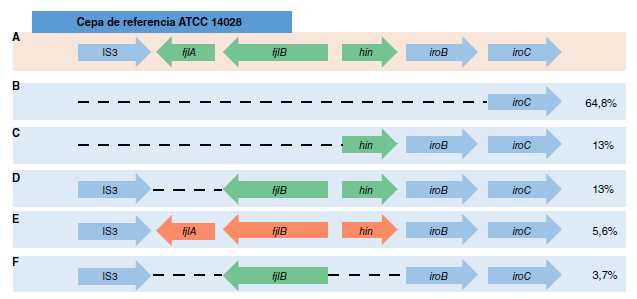
Resultados. El 61 % (n=174) de los aislamientos de Salmonella monofásica correspondió a Salmonella Typhimurium serovar monofásico. El 64,8 % (n=35/54) se relacionó con el clon europeo-español y, el 13 % (n=7/54), con el estadounidense. En dos aislamientos de orina se encontró una diferencia significativa en la motilidad y el crecimiento, así como ausencia de la porina OmpD en medio mínimo M9.
Conclusiones. En el periodo de estudio, circuló en Colombia la variante monofásica de Salmonella Typhimurium relacionada con el clon europeo-español, y se registró ausencia total del operón fljAB. Los resultados evidenciaron cambios fenotípicos en los aislamientos provenientes de muestras de orina que sugieren adaptación en procesos invasivos.
Descargas
Referencias bibliográficas
World Health Organization. Salmonella (no tifoidea). Fecha de consulta: 27 de abril de 2019. Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/salmonella-(nontyphoidal) 2. Grimont PA, Weill FX. Antigenic formulae of the Salmonella serovars. 9th edition. Paris: Institut Pasteur; 2007. p. 166.
Yamamoto S, Kutsukake K. FljA-mediated posttranscriptional control of phase 1 flagellin expression in flagellar phase variation of Salmonella enterica serovar Typhimurium. J Bacteriol. 2006;188:958-67. https://doi.org/10.1128/JB.188.3.958-967.2006
Bonifield HR, Hughes KT. Flagellar phase variation in Salmonella enterica is mediated by a posttranscriptional control mechanism. J Bacteriol. 2003;185:3567-74. https://doi.org/10.1128/JB.185.12.3567-3574.2003
Centers for Disease Control and Prevention (CDC). National Enteric Disease Surveillance. Salmonella Annual Report 2016. Atlanta, USA: CDC; 2018.
European Food Safety Authority and European Centre for Disease Prevention and Control. The European Union One Health 2018 Zoonoses Report. EFSA. 2019;17:e05926.
https://doi.org/10.2903/j.efsa.2019.5926
Arai N, Sekizuka T, Tamamura Y, Tanaka K, Barco L, Izumiya H, et al. Phylogenetic characterization of Salmonella enterica serovar Typhimurium and its monophasic variant isolated from food animals in japan revealed replacement of major epidemic clones in the last 4 decades. J Clin Microbiol. 2018;56:e01758-17. https://doi.org/10.1128/JCM.01758-17
Mastrorilli E, Pietrucci D, Barco L, Ammendola S, Petrin S, Longo A, et al. A comparative genomic analysis provides novel insights into the ecological success of the monophasic salmonella serovar 4,[5],12:i:. Front Microbiol. 2018;9:715. https://doi.org/10.3389/fmicb.2018.00715
Sun H, Wan Y, Du P, Bai L. The epidemiology of monophasic Salmonella typhimurium. Foodborne Pathog Dis 2020;17:87-97. https://doi.org/10.1089/fpd.2019.2676
Hauser E, Tietze E, Helmuth R, Junker E, Blank K, Prager R, et al. Pork contaminated with Salmonella enterica serovar 4,[5],12:i:-, an emerging health risk for humans. Appl Environ Microbiol. 2010;76:4601-10. https://doi.org/10.1128/AEM.02991-09
Soyer Y, Moreno-Switt A, Davis MA, Maurer J, McDonough PL, Schoonmaker-Bopp DJ, et al. Salmonella enterica serotype 4,5,12:i:-, an emerging Salmonella serotype that represents multiple distinct clones. J Clin Microbiol. 2009;47:3546-56. https://doi.org/10.1128/JCM.00546-09
Barco L, Longo A, Lettini AA, Cortini E, Saccardin C, Minorello C, et al. Molecular characterization of “inconsistent” variants of Salmonella Typhimurium isolated in Italy. Foodborne Pathog Dis. 2014;11:497-9. https://doi.org/10.1089/fpd.2013.1714
Rodríguez EC, Díaz-Guevara P, Moreno J, Bautista A, Montaño L, Realpe ME, et al. Laboratory surveillance of Salmonella enterica from human clinical cases in Colombia 2005-2011. Enferm Infecc Microbiol Clin. 2017;35:417-25. https://doi.org/10.1016/j.eimc.2016.02.023
Instituto Nacional de Salud. Vigilancia por laboratorio de Salmonella spp. [Internet]. Bogotá: Instituto Nacional de Salud; 2018.
Li Y, Pulford CV, Díaz P, Pérez-Sepúlveda BM, Duarte C, Predeus AV, et al. Genomic and phylogenetic analysis of Salmonella Typhimurium and its monophasic variants responsible for invasive endemic infections in Colombia. BioRxiv. 2019. https://doi.org/10.1101/588608
Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. 27th edition. CLSI supplement M100. Wayne, PA: CLSI; 2017.
Green MR, Michael R, Sambrook J. Molecular cloning: A laboratory manual. 4th edition. Cold Spring Harbor, N.Y.: Cold Spring Harbor Laboratory Press; 2014.
Pérez-Sepúlveda BM, Heavens D, Pulford CV, Predeus AV, Low R, Webster H, et al. An accessible, efficient and global approach for the large-scale sequencing of bacterial genomes. BioRxiv. 2020. https://doi.org/10.1101/2020.07.22.200840
McClelland M, Sanderson KE, Spieth J, Clifton SW, Latreille P, Courtney L, et al. Complete genome sequence of Salmonella enterica serovar Typhimurium LT2. Nature. 2001;413:852-6. https://doi.org/10.1038/35101614
Echeita MA, Herrera S, Usera MA. Atypical, fljB-negative Salmonella enterica subsp. enterica strain of serovar 4,5,12:i:- appears to be a monophasic variant of serovar Typhimurium. J Clin Microbiol. 2001;39:2981-3. https://doi.org/10.1128/JCM.39.8.2981-2983.2001
Wattam AR, Davis JJ, Assaf R, Boisvert S, Brettin T, Bun C, et al. Improvements to PATRIC, the all-bacterial Bioinformatics Database and Analysis Resource Center. Nucleic Acids Res. 2017;45:D535-42. https://doi.org/10.1093/nar/gkw1017
Bogomolnaya LM, Aldrich L, Ragoza Y, Talamantes M, Andrews KD, McClelland M, et al. Identification of novel factors involved in modulating motility of Salmonella enterica serotype typhimurium. PLoS ONE. 2014;9:e111513. https://doi.org/10.1371/journal.pone.0111513
Villarreal JM, Becerra-Lobato N, Rebollar-Flores JE, Medina-Aparicio L, Carbajal-GómezE, Zavala-García ML, et al. The Salmonella enterica serovar Typhi ltrR-ompR-ompC-ompF genes are involved in resistance to the bile salt sodium deoxycholate and in bacterial transformation. Mol Microbiol. 2014;92:1005-24. https://doi.org/10.1111/mmi.12610
Echeita-Sarrionandia MA, León SH, Baamonde CS. Invasive gastroenteritis, anything new? Enferm Infecc Microbiol Clin. 2011;29(Suppl.3):55-60. https://doi.org/10.1016/S0213-005X(11)70029-5
Hopkins KL, Kirchner M, Guerra B, Granier SA, Lucarelli C, Porrero MC, et al. Multiresistant Salmonella enterica serovar 4,[5],12:i:- in Europe: A new pandemic strain? Euro Surveill. 2010;15:19580.
Cito F, Baldinelli F, Calistri P, Di Giannatale E, Scavia G, Orsini M, et al. Outbreak of unusual Salmonella enterica serovar Typhimurium monophasic variant 1,4 [5],12:i:-, Italy, June 2013 to September 2014. Euro Surveill. 2016;21. https://doi.org/10.2807/1560-7917.ES.2016.21.15.30194
European Food Safety Authority, European Centre for Disease Prevention and Control. The European Union summary report on trends and sources of zoonoses, zoonotic agents and food-borne outbreaks in 2016. EFSA J. 2017;15. https://doi.org/10.2903/j.efsa.2017.5077
Machado J, Bernardo F. Prevalence of Salmonella in chicken carcasses in Portugal. J Appl Bacteriol 1990;69:477-80. https://doi.org/10.1111/j.1365-2672.1990.tb01538.x
Echeita MA, Aladueña A, Cruchaga S, Usera MA. Emergence and spread of an atypical Salmonella enterica subsp. enterica serotype 4,5,12:i:- strain in Spain. J Clin Microbiol. 1999;37:3425. https://doi.org/10.1128/JCM.37.10.3425-3425.1999
Helmuth IG, Espenhain L, Ethelberg S, Jensen T, Kjeldgaard J, Litrup E, et al. An outbreak of monophasic Salmonella Typhimurium associated with raw pork sausage and other pork products, Denmark 2018-19. Epidemiol Infect. 2019;147:e315. https://doi.org/10.1017/S0950268819002073
Magossi G, Bai J, Cernicchiaro N, Jones C, Porter E, Trinetta V. Seasonal presence of Salmonella spp., Salmonella Typhimurium and its monophasic variant serotype I 4,[5],12:i:-, in selected United States Swine Feed Mills. Foodborne Pathog Dis 2019;16:276-81. https://doi.org/10.1089/fpd.2018.2504
Yang X, Wu Q, Zhang J, Huang J, Guo W, Cai S. Prevalence and characterization of monophasic Salmonella serovar 1,4,[5],12:i:- of food origin in China. PLoS ONE. 2015;10:e0137967. https://doi.org/10.1371/journal.pone.0137967
Mulvey MR, Finley R, Allen V, Ang L, Bekal S, El Bailey S, et al. Emergence of multidrugresistant Salmonella enterica serotype 4,[5],12:i:- involving human cases in Canada: Results from the Canadian Integrated Program on Antimicrobial Resistance Surveillance (CIPARS), 2003-10. J Antimicrob Chemother. 2013;68:1982-6. https://doi.org/10.1093/jac/dkt149
Tavechio AT, Fernandes SA, Ghilardi ÂC, Soule G, Ahmed R, Melles CE. Tracing lineage by phenotypic and genotypic markers in Salmonella enterica subsp. enterica serovar 1,4,[5],12:i:- and Salmonella Typhimurium isolated in state of São Paulo, Brazil. Mem Inst Oswaldo Cruz. 2009;104:1042-6. https://doi.org/10.1590/S0074-02762009000700019
Vico JP, Lorenzutti AM, Zogbi AP, Aleu G, Sánchez IC, Caffer MI, et al. Prevalence, associated risk factors, and antimicrobial resistance profiles of non-typhoidal Salmonella in large scale swine production in Córdoba, Argentina. Res Vet Sci. 2020;130:161-9. https://doi.org/10.1016/j.rvsc.2020.03.003
Elnekave E, Hong S, Mather AE, Boxrud D, Taylor AJ, Lappi V, et al. Salmonella enterica serotype 4,[5],12:i:- in Swine in the United States Midwest: An emerging multidrug-resistant clade. Clin Infect Dis. 2018;66:877-85. https://doi.org/10.1093/cid/cix909
de la Torre E, Zapata D, Tello M, Mejía W, Frías N, García-Peña FJ, et al. Several Salmonella enterica subsp. enterica serotype 4,5,12:i:- phage types isolated from swine samples originate from serotype typhimurium DT U302. J Clin Microbiol. 2003;41:2395-400. https://doi.org/10.1128/jcm.41.6.2395-2400.2003
Donado-Godoy P, Clavijo V, León M, Arévalo A, Castellanos R, Bernal J, et al. Counts, serovars, and antimicrobial resistance phenotypes of Salmonella on raw chicken meat at retail in Colombia. J Food Prot. 2014;77:227-35. https://doi.org/10.4315/0362-028X.JFP-13-276
Rodríguez JM, Rondón IS, Verjan N. Serotypes of Salmonella in broiler carcasses marketed at Ibagué, Colombia. Rev Bras Cienc Avic. 2015;17:545-52. https://doi.org/10.1590/1516-635X1704545-552
Rondón-Barragán IS, Arcos EC, Mora-Cardona L, Fandiño C. Characterization of Salmonella species from pork meat in Tolima, Colombia. Revista Colombiana de Ciencias Pecuarias. 2015;28:74-82.
Durango J, Arrieta G, Mattar S. Presencia de Salmonella spp. en un área del Caribe colombiano: un riesgo para la salud pública. Biomédica. 2004;24:89-96. https://doi.org/10.7705/biomedica.v24i1.1252
Petrovska L, Mather AE, AbuOun M, Branchu P, Harris SR, Connor T, et al. Microevolution of monophasic Salmonella Typhimurium during epidemic, United Kingdom, 2005-2010. Emerging Infect Dis. 2016;22:617-24. https://doi.org/10.3201/eid2204.150531
Crayford G, Coombes JL, Humphrey TJ, Wigley P. Monophasic expression of FliC gen by Salmonella 4,[5],12:i:- DT193 does not alter its pathogenicity during infection of porcine intestinal epithelial cells. Microbiology. 2014;160:2507-16. https://doi.org/10.1099/mic.0.081349-0
Tena D, González-Praetorius A, Pérez-Pomata MT, Gimeno C, Alén MJ, Robres P, et al. Urinary infection caused by non typhi Salmonella. Enferm Infecc Microbiol Clin. 2000;18:79-82.
Eriksson S, Lucchini S, Thompson A, Rhen M, Hinton JCD. Unravelling the biology of macrophage infection by gene expression profiling of intracellular Salmonella enterica. Mol Microbiol. 2003;47:103-18. https://doi.org/10.1046/j.1365-2958.2003.03313.x
Ipinza F, Collao B, Monsalva D, Bustamante VH, Luraschi R, Alegría-Arcos M, et al. Participation of the Salmonella OmpD porin in the infection of RAW264.7 macrophages and BALB/c mice. PLoS ONE 2014;9:e111062. https://doi.org/10.1371/journal.pone.0111062
Algunos artículos similares:
- Elizabeth Borrero, Gabriel Carrasquilla, Neal Alexander, Descentralización y reforma: ¿cuál es su impacto sobre la incidencia de malaria en los municipios colombianos? , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Katherine Laiton-Donato, José A. Usme-Ciro, Angélica Rico, Lissethe Pardo, Camilo Martínez, Daniela Salas, Susanne Ardila, Andrés Páez, Análisis filogenético del virus del chikungunya en Colombia: evidencia de selección purificadora en el gen E1 , Biomédica: Vol. 36 (2016): Suplemento 2, Enfermedades virales
- Johnny Durango, Germán Arrieta, Salim Mattar, Presencia de Salmonella spp. en un área del Caribe colombiano: un riesgo para la salud pública. , Biomédica: Vol. 24 Núm. 1 (2004)
- Pablo Chaparro, Edison Soto, Julio Padilla, Daniel Vargas, Estimación del subregistro de casos de paludismo en diez municipios de la costa del Pacífico nariñense durante 2009 , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Nancy Yaneth Flórez , Stefany Alejandra Arévalo , Edna Catering Rodríguez , Jaime Guerrero , Kelly Paola Valverde , Paula Lucía Díaz , Lucy Angeline Montaño, Doris Mabel Gartner , Carolina Duarte , Jaime Enrique Moreno, Brote de Salmonella enterica subsp. enterica serovar Give asociado con enfermedad transmitida por alimentos en Vichada, Colombia, 2015 , Biomédica: Vol. 41 Núm. 1 (2021)
- José Joaquín Carvajal, Nildimar Alves Honorio, Silvia Patricia Díaz, Edinso Rafael Ruiz, Jimmy Asprilla, Susanne Ardila, Gabriel Parra-Henao, Detección de Aedes albopictus (Skuse) (Diptera: Culicidae) en el municipio de Istmina, Chocó, Colombia , Biomédica: Vol. 36 Núm. 3 (2016)
- Myrtha Arango, Elizabeth Castañeda, Clara Inés Agudelo, Catalina De Bedout, Carlos Andrés Agudelo, Angela Tobón, Melva Linares, Yorlady Valencia, Ángela Restrepo, The Colombian Histoplasmosis Study Group, Histoplasmosis en Colombia: resultados de la encuesta nacional, 1992-2008 , Biomédica: Vol. 31 Núm. 3 (2011)
- Yesika del Carmen Rojas, Helena Brochero, Hallazgo de Aedes aegypti (Linnaeus 1762), en el casco urbano del corregimiento de La Pedrera, Amazonas, Colombia , Biomédica: Vol. 28 Núm. 4 (2008)
- Sandra Lorena Girón, Julio César Mateus, Fabián Méndez, Impacto de un botadero a cielo abierto en el desarrollo de síntomas respiratorios y en costos familiares de atención en salud de niños entre 1 y 5 años en Cali, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- Patricia Escobar, Katherine Paola Luna, Indira Paola Hernández, César Mauricio Rueda, María Magdalena Zorro, Simon L. Croft, Susceptibilidad in vitro a hexadecilfosfocolina (miltefosina), nifurtimox y benznidazole de cepas de Trypanosoma cruzi aisladas en Santander, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























