Brote de Salmonella enterica subsp. enterica serovar Give asociado con enfermedad transmitida por alimentos en Vichada, Colombia, 2015
Resumen
Introducción. Salmonella enterica subsp. enterica serovar Give se encuentra en mamíferos rumiantes, cerdos, aves y ambientes acuáticos, pero rara vez en humanos. En Colombia este serotipo ocupó el decimoprimer lugar en frecuencia en la vigilancia por laboratorio de la enfermedad diarreica aguda entre el 2000 y el 2013.
Objetivo. Caracterizar el fenotipo y el genotipo de S. Give en aislamientos relacionados con un brote de enfermedad transmitida por alimentos en el departamento de Vichada en la quinta semana epidemiológica del 2015.
Materiales y métodos. Se buscó Salmonella spp. en 37 muestras de materia fecal con el método de estudio del Instituto Nacional de Salud. La muestra de sardinas enlatadas fue procesada según la norma ISO6579:2002 Cor.1:2004. Se determinó el serotipo en los aislamientos confirmados mediante serología o PCR en tiempo real, y se hicieron pruebas de sensibilidad a antimicrobianos y electroforesis en gel de campo pulsado con las enzimas Xbal y BlnI.
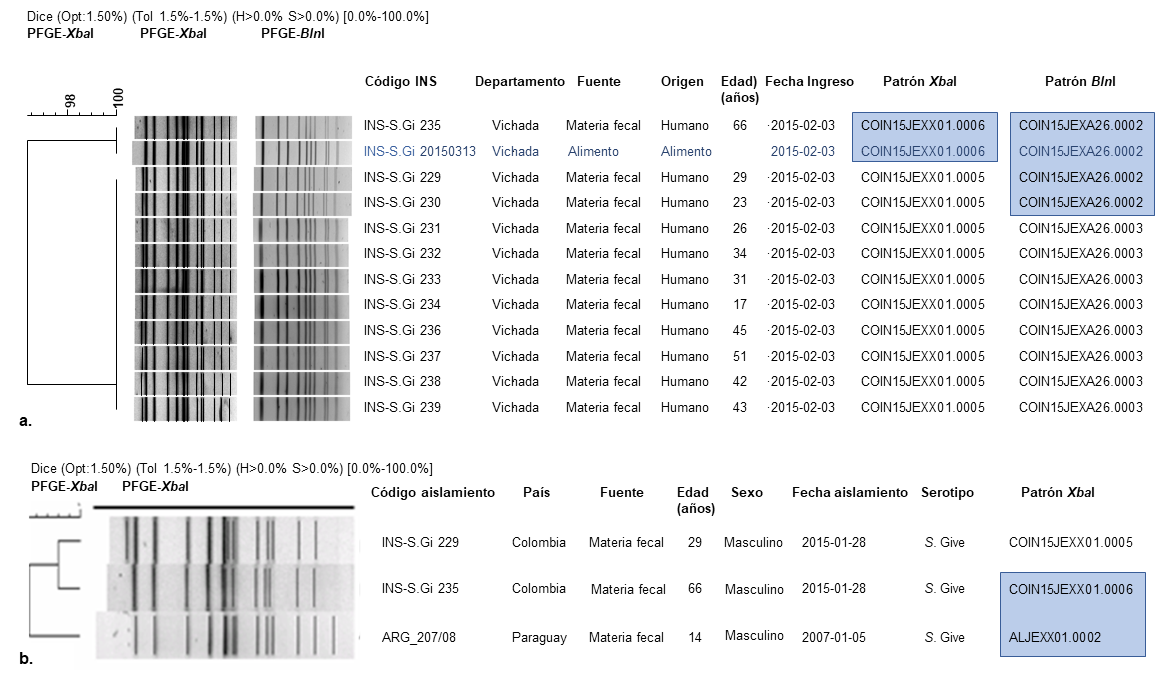
Resultados. Todos los aislamientos de origen humano (11) y el aislamiento del alimento (1), se identificaron como S. Give y este último presentó resistencia a la tetraciclina. El análisis por PFGE-XbaI agrupó bajo el patrón COIN15JEXX01.0005 diez aislamientos de origen humano y a los restantes bajo el COIN15JEXX01.0006, con un 96,3 % de similitud. Los resultados de todos los aislamientos se confirmaron con la enzima BlnI; cuatro de ellos (tres humanos y el del alimento) se agruparon bajo el patrón COIN15JEXA26.002, con un porcentaje de similitud del 95,65 %.
Conclusión. El estudio confirmó que las sardinas enlatadas se relacionaron con la transmisión de S. Give en el brote, que es el tercero ocasionado por este serotipo en Colombia.
Descargas
Referencias bibliográficas
World Health Organization. WHO estimates of the global burden of foodborne diseases: Foodborne disease burden epidemiology reference group 2007-2015. Geneva: WHO; 2015. p. 268.
Guerrero Montilla JA. Informe final del evento enfermedades transmitidas por alimentos, Colombia, 2015. Bogotá: Instituto Nacional de Salud; 2016. p. 17. Fecha de consulta: 5 de septiembre de 2019. Disponible en: https://www.ins.gov.co/buscador-eventos/Informesdeevento/ETA%202015.pdf
Girardin F, Mezger N, Hächler H, Bovier PA. Salmonella serovar Give: An unusual pathogen causing splenic abscess. Eur J Clin Microbiol Infect Dis. 2006;25:272-4. https://doi.org/10.1007/s10096-006-0122-2
Usera MA, Aladueña A, Díez R, Cerdán P, Gutiérrez R, Echeita A. Análisis de los serotipos de de Salmonella sp. aisladas de muestras no humanas en 1996 en España. Boletín Epidemiológico Semanal. España: Instituto de Salud Carlos III; 1997. p. 69-80. Fecha de consulta: 11 de febrero de 2019. Disponible en: http://www.adiveter.com/ftp_public/articulo450.pdf
Jourdan N, Hello S Le, Delmas G, Clouzeau J, Manteau C, Désaubliaux B, et al. Nationwide outbreak of Salmonella enterica serotype Give infections in infants in France, linked to infant milk formula, September 2008. Eurosurveillance. 2008;13:1-2. https://www.eurosurveillance.org/docserver/fulltext/eurosurveillance/13/39/art18994- en.pdf? expires=1613766271&id=id&accname=guest&checksum=E754A4D07E0DF47C1AF 2AAEE2B21FB0E
Borriello G, Lucibelli MG, Pesciaroli M, Carullo MR, Graziani C, Ammendola S, et al. Diversity of Salmonella spp. serovars isolated from the intestines of water buffalo calves with gastroenteritis. BMC Vet Res. 2012;8:1-9. https://doi.org/10.1186/1746-6148-8-201
Maurer JJ, Martín G, Hernández S, Cheng Y, Gerner-Smidt P, Hise KB, et al. Diversity and persistence of Salmonella enterica strains in rural landscapes in the southeastern United States. PLoS ONE. 2015;10:1-19. https://doi.org/10.1371/journal.pone.0128937
Instituto Nacional de Salud. Características de los aislamientos de Salmonella spp. Colombia, Resultados de la vigilancia 2000-2013. p. 1-31. Fecha de consulta: 17 de noviembre de 2019. Disponible en: https://www.ins.gov.co/buscador-eventos/Informacin%20de%20laboratorio/Informe%20Vigilancia%20por%20laboratorio%20de%20Salmonella%20spp%202000-2013.pdf
International Standard ISO. Microbiology of food and animal feeding stuffs - Horizontal method for the detection of Salmonella spp. (ISO 6579:2002). Fecha de consulta: 15 de diciembre de 2016. Disponible en: https://www.iso.org/standard/40377.html
Muñoz N, Díaz-Osorio M, Moreno J, Sánchez-Jiménez M, Cardona-Castro N. Development and evaluation of a multiplex real-time polymerase chain reaction procedure to clinically type prevalent Salmonella enterica serovars. J Mol Diagnostics. 2010;12:220-5. https://doi.org/10.2353/jmoldx.2010.090036
Grimont PA, Weill F-X. Antigenic Formulae of the Salmonella Serovars. 9th edition. WHO Collaborating Centre for Reference and Research on Salmonella, editor. Paris: Institute Pasteur; 2007. p. 1-166.
Caffer MI, Terragno R. Manual de procedimientos para la caracterización de Salmonella. Buenos Aires: Ministerio de Salud; 2001. p. 1-37. Fecha de consulta: 11 de febrero de 2019. Disponible en: https://docplayer.es/12601568-Manual-de-procedimientos-para-lacaracterizacion-de-salmonella.html
Realpe M, Montaño LA. Manual de procedimientos para el diagnóstico bacteriológico de enfermedad diarreica bacteriana aguda, identificación de Salmonella spp., Shigella sp. y Vibrio cholerae. Bogotá: Instituto Nacional de Salud; 2015.
Centers for Disease Control and Prevention. Standard Operating Procedure for PulseNet PFGE of Escherichia coli O157:H7, Escherichia coli non-O157 (STEC), Salmonella serotypes, Shigella sonnei and Shigella flexneri. Internet. CDC PulseNet. PNL05 Last Updated December 2017. p. 1-16. Fecha de consulta: 17 de julio de 2019. Disponible en: https://www.cdc.gov/pulsenet/PDF/ecoli-shigella-salmonella-pfge-protocol-508c.pdf
Roy R, Higgins R, Fortin M, Tardif S. Salmonella Give infection in 2 dairy herds. Can Vet J. 2001;42:468-70.
Jansen A, Frank C, Prager R, Oppermann H, Stark K. Bundesweiter Ausbruch durch Salmonella Give in Deutschland im Jahr 2004. Nation-wide Outbreak of Salmonella Give in Germany, 2004. Z Gastroenterol. 2005;43:707-13. https://doi.org/10.1055/s-2005-858256
Tenover FC, Arbeit RD, Goering R V, Mickelsen PA, Murray BE, Persing DH, et al. Interpreting chromosomal DNA restriction patterns produced by pulsed- field gel electrophoresis: Criteria for bacterial strain typing. J Clin Microbiol. 1995;33:2233-9. https://doi.org/10.1128/JCM.33.9.2233-2239.1995
McClelland M, Jones R, Patel Y, Nelson M. Restriction endonucleases for pulsed field mapping of bacterial genomes. Nucleic Acids Res. 1987;15:5985-6005. https://doi.org/10.1093/nar/15.15.5985
Ribot EM, Fair MA, Gautom R, Cameron DN, Hunter SB, Swaminathan B, et al. Standardization of pulsed-field gel electrophoresis protocols for the subtyping of Escherichia coli O157:H7, Salmonella, and Shigella for PulseNet. Foodborne Pathog Dis. 2006;3:59-67. https://doi.org/10.1089/fpd.2006.3.59
Zheng J, Keys CE, Zhao S, Ahmed R, Meng J, Brown EW. Simultaneous analysis of multiple enzymes increases accuracy of pulsed-field gel electrophoresis in assigning genetic relationships among homogeneous Salmonella strains. J Clin Microbiol. 2011;49:85-94. https://doi.org/10.1128/JCM.00120-10
Goering RV, Tenover FC. Epidemiological interpretation of chromosomal macrorestriction fragment patterns analyzed by pulsed-field gel electrophoresis. J Clin Microbiol. 1997;35:2432-3. https://doi.org/10.1128/JCM.35.9.2432-2433.1997
Galitsopoulou A, Georgantelis D, Kontominas M. The influence of industrial-scale canning on cadmium and lead levels in sardines and anchovies from commercial fishing centres of the Mediterranean Sea. Food Addit Contam Part B Surveill. 2012;5:75-81. https://doi.org/10.1080/19393210.2012.658582
Mol S. Levels of heavy metals in canned bonito, sardines, and mackerel produced in Turkey. Biol Trace Elem Res. 2011;143:974-82. https://doi.org/10.1007/s12011-010-8909-5
Shiber JG. Arsenic, cadmium, lead and mercury in canned sardines commercially available in eastern Kentucky, USA. Mar Pollut Bull. 2011;62:66-72. https://doi.org/10.1016/j.marpolbul.2010.09.008
Castillo A, Mercado I, Lucía LM, Martínez-Ruiz Y, Ponce De León J, Murano EA, et al. Salmonella contamination during production of cantaloupe: A binational study. J Food Prot. 2004;67:713-20. https://doi.org/10.4315/0362-028X-67.4.713
Higgins R, Désilets A, Cantin M, Messier S, Khakhria R, Ismaïl J, et al. Outbreak of Salmonella Give in the Province of Quebec. Can Vet J. 1997;38:780-1.
Jiménez M, Martínez-Urtaza J, Rodríguez-Álvarez MX, León-Felix J, Chaidez C. Prevalence and genetic diversity of Salmonella spp. in a river in a tropical environment in México. J Water Health. 2014;12:874-84. https://doi.org/10.2166/wh.2014.051
Tracogna MF, Lösch LS, Alonso JM, Merino LA. Detection and characterization of Salmonella spp. in recreational aquatic environments in the Northeast of Argentina. Rev Ambient Agua. 2013;8:18-26. https://doi.org/10.4136/ambi-agua.1145
Traoré O, Nyholm O, Siitonen A, Bonkoungou IJO, Traoré AS, Barro N, et al. Prevalence and diversity of Salmonella enterica in water, fish and lettuce in Ouagadougou, Burkina Faso. BMC Microbiol. 2015;15:1-7. https://doi.org/10.1186/s12866-015-0484-7
Fletcher S. Understanding the contribution of environmental factors in the spread of antimicrobial resistance. Environ Health Prev Med. 2015;20:243-52. https://doi.org/10.1007/s12199-015-0468-0
Molina A, Granados-Chinchilla F, Jiménez M, Acuña-Calvo MT, Alfaro M, Chavarría G. Vigilance for Salmonella in feedstuffs available in Costa Rica: Prevalence, serotyping and tetracycline resistance of isolates obtained from 2009 to 2014. Foodborne Pathog Dis. 2016;13:119-27. https://doi.org/10.1089/fpd.2015.2050
González F, Araque M. Association of transferable quinolone resistance determinant qnrB19 with extended-spectrum β-lactamases in Salmonella Give and Salmonella Heidelberg in Venezuela. Int J Microbiol. 2013;2013:6. https://doi.org/10.1155/2013/628185
Chinen I, Campos J, Dorji T, Pérez-Gutiérrez E. PulseNet Latin America and the Caribbean Network: Present and future. Foodborne Pathog Dis. 2019;16:489-97. https://doi.org/10.1089/fpd.2018.2587
Algunos artículos similares:
- Johnny Durango, Germán Arrieta, Salim Mattar, Presencia de Salmonella spp. en un área del Caribe colombiano: un riesgo para la salud pública. , Biomédica: Vol. 24 Núm. 1 (2004)
- Elizabeth Borrero, Gabriel Carrasquilla, Neal Alexander, Descentralización y reforma: ¿cuál es su impacto sobre la incidencia de malaria en los municipios colombianos? , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Katherine Laiton-Donato, José A. Usme-Ciro, Angélica Rico, Lissethe Pardo, Camilo Martínez, Daniela Salas, Susanne Ardila, Andrés Páez, Análisis filogenético del virus del chikungunya en Colombia: evidencia de selección purificadora en el gen E1 , Biomédica: Vol. 36 (2016): Suplemento 2, Enfermedades virales
- Pablo Chaparro, Edison Soto, Julio Padilla, Daniel Vargas, Estimación del subregistro de casos de paludismo en diez municipios de la costa del Pacífico nariñense durante 2009 , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Paloma Cuenca-Arias , Lucy Angeline Montaño , José Miguel Villarreal , Magdalena Wiesner, Caracterización molecular y fenotípica de aislamientos clínicos de Salmonella Typhimurium variante monofásica (1,4,[5],12:i:-) recuperados en Colombia , Biomédica: Vol. 40 Núm. 4 (2020)
- José Joaquín Carvajal, Nildimar Alves Honorio, Silvia Patricia Díaz, Edinso Rafael Ruiz, Jimmy Asprilla, Susanne Ardila, Gabriel Parra-Henao, Detección de Aedes albopictus (Skuse) (Diptera: Culicidae) en el municipio de Istmina, Chocó, Colombia , Biomédica: Vol. 36 Núm. 3 (2016)
- Myrtha Arango, Elizabeth Castañeda, Clara Inés Agudelo, Catalina De Bedout, Carlos Andrés Agudelo, Angela Tobón, Melva Linares, Yorlady Valencia, Ángela Restrepo, The Colombian Histoplasmosis Study Group, Histoplasmosis en Colombia: resultados de la encuesta nacional, 1992-2008 , Biomédica: Vol. 31 Núm. 3 (2011)
- Yesika del Carmen Rojas, Helena Brochero, Hallazgo de Aedes aegypti (Linnaeus 1762), en el casco urbano del corregimiento de La Pedrera, Amazonas, Colombia , Biomédica: Vol. 28 Núm. 4 (2008)
- Sandra Lorena Girón, Julio César Mateus, Fabián Méndez, Impacto de un botadero a cielo abierto en el desarrollo de síntomas respiratorios y en costos familiares de atención en salud de niños entre 1 y 5 años en Cali, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- Patricia Escobar, Katherine Paola Luna, Indira Paola Hernández, César Mauricio Rueda, María Magdalena Zorro, Simon L. Croft, Susceptibilidad in vitro a hexadecilfosfocolina (miltefosina), nifurtimox y benznidazole de cepas de Trypanosoma cruzi aisladas en Santander, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























