Protocolo rápido y económico para la producción de antígenos de Paracoccidioides spp.
Resumen
Introducción. Los métodos existentes para la producción de los antígenos de Paracoccidioides spp. son problemáticos en su estandarización, especificidad, estabilidad, repetibilidad y reproducibilidad.
Objetivo. Optimizar la metodología para la producción de antígenos de Paracoccidioides spp. y evaluar su aplicabilidad en el inmunodiagnóstico de la paracoccidioidomicosis.
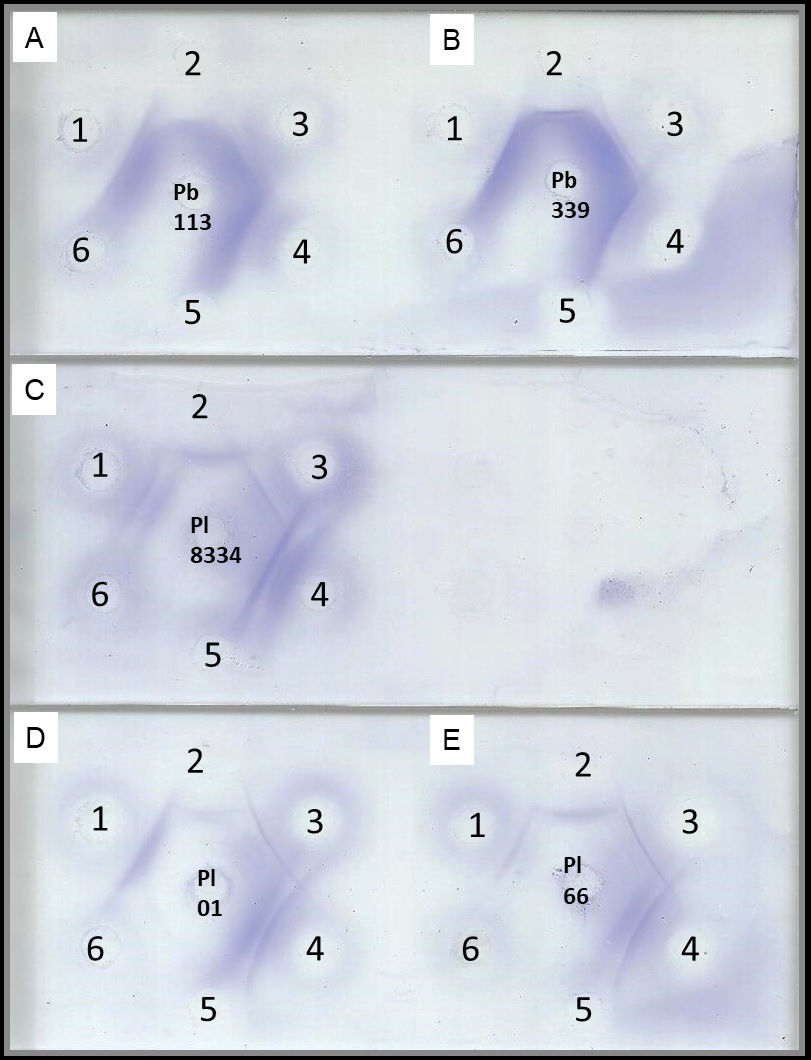
Materiales y métodos. Los antígenos se obtuvieron de aislamientos de P. lutzii (01, 66 y 8334), P. brasiliensis sensu stricto (113) y P. restripiensis (B-339). Estos hongos se cultivaron a 36 °C ± 1 °C en agar Fava-Netto modificado, según Freitas et al. (2018). Los antígenos de P. lutzii se obtuvieron a los 5, 10 y 20 días de cultivo y los antígenos de P. brasiliensis y P. restripiensis se obtuvieron a los 10 días. Los antígenos se evaluaron in natura, concentrados 10 y 20 veces. La capacidad antigénica se evaluó mediante un ensayo de inmunodifusión doble con muestras de suero de pacientes con paracoccidioidomicosis, histoplasmosis, aspergilosis y donantes de sangre aleatorios.
Resultados. Se observó reacción cruzada con Paracoccidioides spp. cuando se evaluaron los antígenos de P. brasiliensis, P. restrepiensis y P. lutzii frente a los anticuerpos policlonales contra P. lutzii y P. brasiliensis, respectivamente. No hubo reactividad cruzada con los anticuerpos policlonales contra Histoplasma capsulatum y Aspergillus fumigatus, ni contra los donantes de sangre aleatorios. El protocolo propuesto permitió la producción estable, repetible y reproducible de antígenos dirigidos de un género específico (Paracoccidiodes) en un tiempo corto de cultivo y a un menor costo.
Conclusión. El protocolo propuesto permitió obtener antígenos específicos de un género, que pueden ser desarrollados y reproducidos en todos los laboratorios de Brasil y Surámerica donde la paracoccidioidomicosis es una enfermedad endémica y desatendida. Estos antígenos pueden contribuir al diagnóstico precoz de la infección, independientemente de la especie.
Descargas
Referencias bibliográficas
Gonzalez A, Hernandez O. New insights into a complex fungal pathogen: the case of Paracoccidioides spp. Yeast. 2016;33:113-28. https://doi.org/10.1002/yea.3147
Queiroz-Telles F, Fahal AH, Falci DR, Caceres DH, Chiller T, Pasqualotto AC. Neglected endemic mycoses. Lancet Infect Dis. 2017;17:e377. https://doi.org/10.1016/S1473-3099(17)30306-7
Shikanai-Yasuda MA, Mendes RP, Colombo AL, Queiroz-Telles F, Kono ASG, Paniago AMM, et al. Brazilian guidelines for the clinical management of paracoccidioidomycosis. Rev Soc Bras Med Trop. 2017;50:715-40. https://doi.org/10.1590/0037-8682-0230-2017
Martinez, R. New trends in Paracoccidioidomycosis epidemiology. J Fungi. 2017;3:1. https://doi.org/10.3390/jof3010001
Mendes RP, Cavalcante RS, Marques SA, Marques MEA, Venturini J, Sylvestre TF. Paracoccidioidomycosis: Current perspectives from Brazil. Open Microbiol J. 2017;31:224-82. https://doi.org/10.2174/1874285801711010224
da Silva JF, de Oliveira HC, Marcos CM, Assato PA, Fusco-Almeida AM, Mendes-Giannini MJ. Advances and challenges in paracoccidioidomycosis serology caused by Paracoccidioides species complex: an update. Diagn Microbiol Infect Dis. 2016;8487-94. https://doi.org/10.1016/j.diagmicrobio.2015.06.004
Ferreira CS, Ribeiro EMC, Goes AM, Silva BM. Current strategies for diagnosis of paracoccidioidomycosis and prospects of methods based on gold nanoparticles. Future Microbiol. 2016;11:973-85. https://doi.org/10.2217/fmb-2016-0062
Almeida-Paes R, Bernardes-Engemann AR, da Silva Motta B, Pizzini CV, de Abreu Almeida M, de Medeiros Muniz M, et al. Immunologic diagnosis of endemic mycoses. J Fungi (Basel). 2022;8:993. https://doi.org/10.3390/jof8100993
Peçanha PM, Peçanha-Pietrobom PM, Grão-Velloso TR, Rosa Júnior M, Falqueto A, Gonçalves SS. Paracoccidioidomycosis: What we know and what is new in epidemiology, diagnosis, and treatment. J Fungi (Basel). 2022;8:1098. https://doi.org/10.3390/jof8101098
Kamikawa CM, Mendes RP, Vicentini AP. Standardization and validation of Dot-ELISA assay for Paracoccidioides brasiliensis antibody detection. J Venom Anim Toxins Incl Trop Dis. 2017;23:11. https://doi.org/10.1186/s40409-017-0101-3
Vidal MS, Del Negro GM, Vicentini AP, Svidzinski TI, Mendes-Giannini MJ, Almeida AM, et al. Serological diagnosis of paracoccidioidomycosis: high rate of inter-laboratorial variability among medical mycology reference centers. PLoS Negl Trop Dis. 2014;8:e3174. https://doi.org/10.1371/journal.pntd.0003174
de Camargo ZP. Serology of paracoccidioidomycosis. Mycopathologia. 2008;165:289-302. https://doi.org/10.1007/s11046-007-9060-5
de Freitas RS, Kamikawa CM, Vicentini AP. Fast protocol for the production of Histoplasma capsulatum antigens for antibody detection in the immunodiagnosis of histoplasmosis. Rev Iberoam Micol. 2018;35:27-31. https://doi.org/10.1016/j.riam.2017.04.004
Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976;72:248-54. https://doi.org/10.1006/abio.1976.9999
Ouchterlony O. Antigen-antibody reactions in gels. Acta Pathol Microbiol Scand. 1949;26:507-15. https://doi.org/10.1111/j.1699-0463.1949.tb00751.x
Laemmli UK. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature.1970;227:680-5. https://doi.org/10.1038/227680a0
Ansorge W. Fast and sensitive detection of protein and DNA bands by treatment with potassium permanganate. J Biochem Biophys Methods. 1985;11:13-20. https://doi.org/10.1016/0165-022x(85)90037-5
Vicentini-Moreira AP. Paracoccidioidomicose: histórico, etiologia, epidemiologia, patogênese, formas clínicas, diagnóstico laboratorial e antígenos. Bol Epidemiol Paul. 2008;5:11-24.
Gegembauer G, Araujo LM, Pereira EF, Rodrigues AM, Paniago AM, Hahn RC, et al. Serology of paracoccidioidomycosis due to Paracoccidioides lutzii. PLoS Negl Trop Dis 2014;8:e2986. https://doi.org/10.1371/journal.pntd.0002986
Queiroz Junior LDP, de Camargo ZP, Tadano T, Rodrigues AM, Takarara DT, Gegembauer G, et al. Serological and antigenic profiles of clinical isolates of Paracoccidioides spp. from Central Western Brazil. Mycoses. 2014;57:466-72. https://doi.org/10.1111/myc.12183
de Camargo ZP, de Franco MF. Current knowledge on pathogenesis and immunodiagnosis of paracoccidioidomycosis. Rev Iberoam Micol. 2000;17:41-8.
Camargo ZP, Berzaghi R, Amaral CC, Silva SH. Simplified method for producing Paracoccidioides brasiliensis exoantigens for use in immunodiffusion tests. Med Mycol. 2003;41:539-42. https://doi.org/10.1080/13693780310001615358
Leitão NP Jr, Vallejo MC, Conceição PM, Camargo ZP, Hahn R, Puccia R. Paracoccidioides lutzii Plp43 is an active glucanase with partial antigenic identity with P. brasiliensis gp43. PLoS Negl Trop Dis. 2014;8:e3111. https://doi.org/10.1371/journal.pntd.0003111
Arantes TD, Theodoro RC, Teixeira M de M, Bosco S de M, Bagagli E. Environmental mapping of Paracoccidioides spp. in Brazil reveals new clues into genetic diversity, biogeography and wild host association. PLoS Negl Trop Dis. 2016;10:e0004606. https://doi.org/10.1371/journal.pntd.0004606
Mendes JF, Klafke GB, Albano APN, Cabana AL, Teles AJ, de Camargo ZP, et al. Paracoccidioidomycosis infection in domestic and wild mammals by Paracoccidioides lutzii. Mycoses. 2017;60:402-6. https://doi.org/10.1111/myc.12608
Buccheri R, Morais VDS, Kamikawa CM, Vidal MSM, Naves G, Del Negro GMB, et al. Case Report: misleading serological diagnosis of paracoccidioidomycosis in a young patient with the acute form disease: Paracoccidioides brasiliensis or Paracoccidioides lutzii? Am J Trop Med Hyg. 2018;98:1082-5. https://doi.org/10.4269/ajtmh.17-0812
Lenhard-Vidal A, Assolini JP, Chiyoda FAS, Ono MA, Sano A, Itano EN. Polyclonal antibodies to Paracoccidioides brasiliensis are able to recognise antigens from different strains from Paracoccidioides species complex, including Paracoccidioides lutzii LDR2. Mycoses. 2018;61:826-32. https://doi.org/10.1111/myc.12819
Do Valle ACF, Costa RLB, Fialho Monteiro PC, Von Helder J, Muniz MM, Zancopé-Oliveira RM. Interpretation and clinical correlation of serological tests in paracoccidioidomycosis. Med Mycol. 2001;39:373-7. https://doi.org/10.1080/mmy.39.4.373.37
Torres Esteche V, Arteta Z, Torres G, Vaucher A, Gezuele E, Balleste R. Concomitant pulmonary paracoccidioidomycosis and pulmonary histoplasmosis: a rare case. J Bras Pneumol. 2012;38:264-8. https://doi.org/10.1590/s1806-37132012000200017
Fernandes VC, Coitinho JB, Veloso JM, Araújo SA, Pedroso EP, Goes AM. Combined use of Paracoccidioides brasiliensis recombinant rPb27 and rPb40 antigens in an enzyme-linke immunosorbent assay for immunodiagnosis of paracoccidioidomycosis. J Immunol Methods. 2011;367:78-84. https://doi.org/10.1016/j.jim.2011.02.006
Kamikawa CM, Vicentini AP. Multiparametric assay of screening for the diagnosis of mycoses of interest in Public Health: standardization of methodology. Rev Inst Adolfo Lutz. 2022;81:1-11,e37165. https://doi.org/10.53393/rial.2022.v.81.37165
Dos Santos PO, Rodrigues AM, Fernandes GF, da Silva SH, Burger E, de Camargo ZP. Immunodiagnosis of paracoccidioidomycosis due to Paracoccidioides brasiliensis using a latex test: detection of specific antibody anti-gp43 and specific antigen gp43. PLoS Negl Trop Dis. 2015;13:e0003516. https://doi.org/10.1371/journal.pntd.0003516
Ortiz BL, Díez S, Urán ME, Rivas JM, Romero M, Caicedo, et al. Use of the 27-kilodalton recombinant protein from Paracoccidioides brasiliensis in serodiagnosis of paracoccidioidomycosis. Clin Diagn Lab Immunol. 1998;5:826-30. https://doi.org/10.1128/CDLI.5.6.826-830.1998
Algunos artículos similares:
- Ana María García, Orville Hernández, Beatriz H. Aristizábal, Luz Elena Cano, Juan G. McEwen, Ángela Restrepo, Identificación de algunos genes asociados al proceso de germinación de la conidia al micelio en Paracoccidioides brasiliensis , Biomédica: Vol. 29 Núm. 3 (2009)
- Orville Hernández, Diana Tamayo, Isaura Torres, Ángela Restrepo, Juan Guillermo McEwen, Ana María García, Análisis de la cinética de expresión de genes durante la transición de micelio a levadura y la germinación levadura a micelio en Paracoccidioides brasiliensis , Biomédica: Vol. 31 Núm. 4 (2011)
- Angélica Ballesteros, Sandra Beltrán, Jaime Patiño, Cynthia Bernal, Rocío Orduz, Paracoccidioidomicosis juvenil diseminada diagnosticada en una niña en área urbana , Biomédica: Vol. 34 Núm. 1 (2014)
- Lina M. Osorio-Cock, Sandra Catalina Jaramillo-Pulgarín, Alba P. Ferrín-Bastidas, Diana Y. Molina-Colorado, Óscar M. Gómez-Guzmán, Alejandra Zuluaga, Juan G. McEwen-Ochoa, Martha E. Urán-Jiménez, María del Pilar Jiménez-Alzate, Hiperplasia pseudoepiteliomatosa: carcinoma escamocelular versus paracoccidioidomicosis oral, un caso con mirada dermatológica , Biomédica: Vol. 43 Núm. Sp. 1 (2023): Agosto, Micología médica
- Norma B. Fernández, Adriana Toranzo, Luciana Farias, Cristina E. Canteros, Diagnóstico micológico de paracoccidioidomicosis en un hospital de área no endémica: metodología clásica y molecular , Biomédica: Vol. 43 Núm. Sp. 1 (2023): Agosto, Micología médica
Derechos de autor 2023 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























