Seroprevalencia de arbovirus en Ecuador: implicaciones para mejorar su vigilancia
Resumen
Introducción. Los virus transmitidos por artrópodos (arbovirus) causan morbilidad y mortalidad en humanos y animales domésticos mundialmente. Se desconoce el porcentaje de inmunidad o vulnerabilidad de la población ecuatoriana ante estos virus.
Objetivos. Investigar la proporción de poblaciones ecuatorianas con anticuerpos IgG (exposición o inmunidad pasada) y anticuerpos IgM (exposición reciente) contra flavivirus y alfavirus, e investigar su actividad en Ecuador.
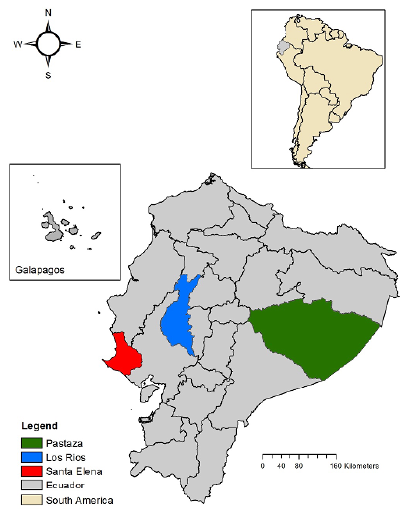
Materiales y métodos. Entre 2009 y 2011, se llevó a cabo una encuesta serológica para arbovirus en humanos (n=1.842), equinos (n=149) y hámsters centinela (n=84) en dos localidades costeras y en una en la Amazonía, utilizando la prueba ELISA (Enzyme-Linked ImmunoSorbent Assay) y la prueba de inhibición de la hemaglutinación.
Resultados. Entre el 20,63 y el 63,61 % de los humanos registraron IgG contra el virus del dengue (DENV), el de la fiebre amarilla (YFV), el de la encefalitis de San Luis y el del Nilo Occidental (WNV); entre 4,67 y 8,63 % tenían IgG para los virus de la encefalitis equina venezolana, de la encefalitis equina del este y de la encefalitis equina del oeste. Se encontró IgM para DENV y WNV. En los equinos y en los hámsters se encontraron anticuerpos contra alfavirus en todas las localidades muestreadas; dos hámsters mostraron seroconversión a YFV en la Amazonía.
Conclusiones. Los resultados del estudio evidenciaron los antecedentes de vacunación contra el YFV y sugieren la actividad de arbovirus no incluidos en el esquema de vigilancia actual. Se recomienda ampliar la vigilancia de arbovirus y mosquitos, continuar con la vacunación contra el YFV, y evaluar su cobertura y efectividad.
Descargas
Referencias bibliográficas
Gubler DJ, Vasilakis N. The Arboviruses: Quo Vadis? Norfolk: Caister Academic Press; 2016. p. 1-6. https://doi.org/10.21775/9781910190210.01
Wilder-Smith A, Gubler DJ, Weaver SC, Monath TP, Heymann DL, Scott TW. Epidemic arboviral diseases: Priorities for research and public health. Lancet Infect. Dis. 2017;17:e101-6. https//doi.org/10.1016/S1473-3099(16)30518-7
Karabatsos N. International catalogue of arboviruses, including certain other viruses of vertebrates. San Antonio, Tex.: American Society of Tropical Medicine and Hygiene for the Subcommittee on Information Exchange of the American Committee on Arthropod-borne Viruses; 1985.
Mayer SV, Tesh RB, Vasilakis N. The emergence of arthropod-borne viral diseases: A global prospective on dengue, chikungunya and zika fevers. Acta Trop. 2017;166:155-63. https//doi.org/10.1016/j.actatropica.2016.11.020
Borja Lavayen C. La fiebre amarilla. Apuntes sobre la epidemia de 1880. In: La fiebre amarilla y los médicos de Guayaquil. Quito: Banco Central del Ecuador; 1987. p. 11-81.
Alava AA, Mosquera C, Vargas W, Real J. Dengue en el Ecuador 1989-2002. Rev Ecuat Hig Med Trop. 2005;42:11-34.
Gutiérrez VE, Monath TP, Alava AA, Uriguen BD, Arzube RM, Chamberlain R. Epidemiologic investigations of the 1969 epidemic of Venezuelan encephalitis in Ecuador. Am J Epidemiol. 1975;102:400-13.
Dirección Nacional de Vigilancia Epidemiológica-MSP. Enfermedades transmitidas por vectores. Fiebre Chikungunya. Semana epidemiológica 52/2018. Accessed: August 15, 2020. Available from: https://www.salud.gob.ec/wp-content/uploads/2019/01/GACETA-VECTORES-SE-52.pdf
Dirección Nacional de Vigilancia Epidemiológica-MSP. Zika. Semana epidemiológica 52/2018. Accessed: August 15, 2020. Available from: https://www.salud.gob.ec/wp-content/uploads/2019/01/GACETA-VECTORES-SE-52.pdf
Monath TP. Yellow fever: An update. Lancet Infect Dis. 2001;1:11-20. https//doi.org/10.1016/S1473-3099(01)00016-0
Becerra L. Informe del Director de Sanidad Pública. N 195. Al Ministro de lo Interior y Sanidad. Guayaquil 27 de mayo. In: Guayaquil: 1740-1919 Crónica y reflexiones epidemiológicas sobre la fiebre amarilla en la ciudad. Guayaquil: Facultad de Ciencias Psicológicas, Universidad de Guayaquil; 2004. p. 165-6.
García E. La fiebre amarilla en Ecuador. Rev Ecuat Hig Med Trop. 1953;10:1-7.
Dirección Nacional de Vigilancia Epidemiológica-MSP. Enfermedades transmitidas por vectores Ecuador, SE 01- 27 - 2020. Accessed: August 16, 2020. Available from: https://www.salud.gob.ec/wp-content/uploads/2020/07/ETV-SE-27.pdf
Dirección Nacional de Vigilancia Epidemiológica-MSP. Enfermedades transmitidas por vectores. Dengue. SE01-31/2020. Accessed: August 15, 2020. Available from https://www.salud.gob.ec/wp-content/uploads/2020/08/Vectores-SE-31.pdf
Gutiérrez VE. Encefalitis venezolana en el Ecuador. Brote epizoodémico de 1972. Rev Ecuat Hig Med Trop. 1977;30:169-88.
Centers for Disease Control and Prevention (CDC). Venezuelan equine encephalitis. Arbovirus Catalog. Accessed: August 15, 2020. Available from: https://wwwn.cdc.gov/arbocat/VirusDetails.aspx?ID=507&SID=10
Young NA. Origin of epidemics of Venezuelan equine encephalitis. J Infect Dis. 1972;125:565-7.
Kinney RM, Tsuchiya KR, Sneider JM, Trent DW. Molecular evidence for the origin of the widespread Venezuelan equine encephalitis epizootic of 1969 to 1972. J Gen Virol. 1992;73:3301-5. https//doi.org/10.1099/0022-1317-73-12-3301
Weaver SC, Pfeffer M, Marriott K, Kang W, Kinney RM. Genetic evidence for the origins of Venezuelan equine encephalitis virus subtype IAB outbreaks. Am J Trop Med Hyg. 1999;60:441-8. https//doi.org/10.4269/ajtmh.1999.60.441
Calisher CH, Gutiérrez VE, Francy DB, Alava AA, Muth DJ, Lazuick JS. Identification of hitherto unrecognized arboviruses from Ecuador: Members of serogroups B, C, Bunyamwera, Patois, and Minatitlan. Am J Trop Med Hyg. 1983;32:877-85. https//doi.org/10.4269/ajtmh.1983.32.877
Coello R. Presencia del virus del Nilo occidental en equinos (Equus caballus) de doshumedales de la Provincia de los Ríos, año 2007 al 2009. Revista de la Universidad de Guayaquil. 2011;111:15-22.
Johnson BW, Cruz C, Felices V, Espinoza WR, Manock SR, Guevara C, et al. Ilheus virus isolate from a human, Ecuador. Emerg Infect Dis. 2007;13:956. https//doi.org/10.3201/eid1306.070118
Izurieta R, Macaluso M, Watts D, Tesh R, Guerra B, Cruz L, et al. Hunting in the rainforest and Mayaro virus infection: An emerging alphavirus in Ecuador. J Glob Infect Dis. 2011;3:317. ttps//doi.org/10.4103/0974-777x.91049
Wise EL, Pullan ST, Márquez S, Paz V, Mosquera JD, Zapata S, et al. Isolation of oropouche virus from febrile patient, Ecuador. Emerg Infect Dis. 2018;24:935. https//doi.org/10.3201/eid2405.171569
Manock SR, Jacobsen KH, De Bravo NB, Russell KL, Negrete M, Olson JG, et al. Etiology of acute undifferentiated febrile illness in the Amazon basin of Ecuador. Am J Trop Med Hyg. 2009;81:146-51.
World Organization for Animal Health-OIE. Encefalomielitis equina del este, Ecuador. 2013. Accessed: August 15, 2020. Available from: https://www.oie.int/wahis_2/public/wahid.php/Reviewreport/Review?page_refer=MapFullEventReport&reportid=13534&newlang=es
Groseth A, Vine V, Weisend C, Guevara C, Watts D, Russell B, et al. Maguari virus associated with human disease. Emerg Infect Dis. 2017;23:1325. https//doi.org/10.3201/eid2308.161254
Metcalf CJE, Farrar J, Cutts FT, Basta NE, Graham AL, Lessler J, et al. Use of serological surveys to generate key insights into the changing global landscape of infectious disease. Lancet. 2016;388:728-30. https//doi.org/10.1016/S0140-6736(16)30164-7
Beaty BJ, Calisher CH, Shope RE. Arboviruses. En: Lennette EH, Lennette DA, Lennette ET, editors. Diagnostic procedures for viral, rickettsial, and chlamydial infections. 7th edition. Washington: American Public Health Association 1995; p.189-212.
Sudia WD, Chamberlain RW. Battery-operated light trap, an improved model. Mosq News. 1962;22:126-9.
Johnson AJ, Martin DA, Karabatsos N, Roehrig JT. Detection of anti-arboviral immunoglobulin G by using a monoclonal antibody-based capture enzyme-linked immunosorbent assay. J Clin Microbiol. 2000;38:1827-31. https//doi.org/10.1128/JCM.38.5.1827-1831.2000
Casals J. Immunological techniques for animal viruses. In: Methods in virology. New York: Elsevier; 1967. p. 113-98. https://doi.org/10.1016/B978-1-4832-3219-5.50010-X
Instituto de Medicina Tropical Pedro Kouri. Técnicas de laboratorio para el diagnóstico y la caracterización de los virus del dengue. Habana: Instituto de Medicina Tropical “Pedro Kourí”; 2013.
Sudia WD, Lord RD, Hayes RO. Collection and processing of vertebrate specimens for arbovirus studies. Atlanta: US Department of Health, Education and Welfare; 1970. p. 28-46.
Ayers M, Adachi D, Johnson G, Andonova M, Drebot M, Tellier R. A single tube RT-PCR assay for the detection of mosquito-borne flaviviruses. J Virol Methods. 2006;135:235-9. https//doi.org/10.1016/j.jviromet.2006.03.009
Sánchez-Seco MP, Rosario D, Quiroz E, Guzmán G, Tenorio A. A generic nested-RT-PCR followed by sequencing for detection and identification of members of the alphavirus genus. J Virol Methods. 2001;95:153-61. https//doi.org/10.1016/S0166-0934(01)00306-8
Eastwood G, Goodman SJ, Hilgert N, Cruz M, Kramer LD, Cunningham AA. Using avian surveillance in Ecuador to assess the imminence of West Nile virus incursion to Galápagos. Ecohealth. 2014;11:53-62. https//doi.org/10.1007/s10393-014-0911-5
Guerra HL, Sardinha TM, da Rosa AP, Lima e Costa MF. Effectiveness of the yellow fever vaccine 17D: An epidemiologic evaluation in health services. Rev Panam Salud Pública. 1997;2:115-20.
Staples JE, Gershman M, Fischer M. Yellow fever vaccine: Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2010:59;1-27.
World Health Organization. Ecuador: WHO and UNICEF estimates of immunization coverage: 2019 revision. Accessed: August 15, 2020. Available from: https://www.who.int/immunization/monitoring_surveillance/data/ecu.pdf
Shearer FM, Moyes CL, Pigott DM, Brady OJ, Marinho F, Deshpande A, et al. Global yellow fever vaccination coverage from 1970 to 2016: An adjusted retrospective analysis. Lancet Infect Dis. 2017;17:1209-17. https//doi.org/10.1016/S1473-3099(17)30419-X
Franck PT, Johnson KM. An outbreak of Venezuelan equine encephalomyelitis in Central America: Evidence for exogenous source of a virulent virus subtype. Am J Epidemiol. 1971;94:487-95. https//doi.org/10.1093/oxfordjournals.aje.a121346
Rico-Hesse R, Weaver SC, De Siger J, Medina G, Salas RA. Emergence of a new epidemic/epizootic Venezuelan equine encephalitis virus in South America. Proc Natl Acad Sci. 1995;92:5278-81. https//doi.org/10.1073/pnas.92.12.5278
Forrester NL, Wertheim JO, Dugan VG, Auguste AJ, Lin D, Adams AP, et al. Evolution and spread of Venezuelan equine encephalitis complex alphavirus in the Americas. PLoS Negl Trop Dis. 2017;11:e0005693. https//doi.org/10.1371/journal.pntd.0005693
Arrigo NC, Adams AP, Weaver SC. Evolutionary patterns of eastern equine encephalitis virus in North versus South America suggest ecological differences and taxonomic revision. J Virol. 2010;84:1014-25. https//doi.org/10.1128/JVI.01586-09
Carrera JP, Forrester N, Wang E, Vittor AY, Haddow AD, Loṕez-Vergès S, et al. Eastern equine encephalitis in Latin America. N Engl J Med. 2013;22;369:732-44. https//doi.org/10.1056/NEJMoa1212628
Espinal MA, Andrus JK, Jauregui B, Waterman SH, Morens DM, Santos JI, et al. Emerging and reemerging aedes-transmitted arbovirus infections in the region of the Americas: Implications for health policy. Am J Public Health. 2019;109:387-92. https//doi.org/10.2105/AJPH.2018.304849
Calisher CH, Blair CD, Bowen MD, Casals J, Drebot MA, Henchal EA, et al. Identification of arboviruses and certain rodent-borne viruses: Reevaluation of the paradigm. Emerg Infect Dis. 2001;7:756. https//doi.org/10.3201/eid0704.010431
Faria NR, Kraemer MU, Hill SC, De Jesus JG, Aguiar RS, Iani FC, et al. Genomic and epidemiological monitoring of yellow fever virus transmission potential. Science. 2018;361:894-9. https//doi.org/1126/science.aat7115
Holmes EC. RNA virus genomics: A world of possibilities. J Clin Invest. 2009;119:2488-95. https//doi.org/10.1172/JCI38050
Coffey LL, Page BL, Greninger AL, Herring BL, Russell RC, Doggett SL, et al. Enhanced arbovirus surveillance with deep sequencing: Identification of novel rhabdoviruses and bunyaviruses in Australian mosquitoes. Virology. 2014;448:146-58. https//doi.org/10.1016/j.virol.2013.09.026
Miranda JJ, Castro-Ávila AC, Salicrup LA. Advancing health through research partnerships in Latin America. BMJ. 2018;16;362:k2690. https//doi.org/10.1136/bmj.k2690
Algunos artículos similares:
- Raúl A. Rojo-Ospina, Marcela Quimbayo-Forero, Arley Calle-Tobón, Sindy C. Bedoya-Patiño, Maribel Gómez, Astrid Ramírez, Johnny Sánchez, Juan F. Silva-Alzate, Carlos J. Montes-Zuluaga, Jorge M. Cadavid, Enrique A. Henao-Correa, El programa del manejo integrado de vectores en el marco de la pandemia por COVID-19 en Medellín, Colombia , Biomédica: Vol. 43 Núm. 1 (2023)
- Eliana Patricia Calvo, Carolina Coronel-Ruiz, Syrley Velazco, Myriam Velandia-Romero, Jaime E. Castellanos, Diagnóstico diferencial de dengue y chikungunya en pacientes pediátricos , Biomédica: Vol. 36 (2016): Suplemento 2, Enfermedades virales
- Jorge R. Rey, Philip Lounibos, Ecología de Aedes aegypti y Aedes albopictus en América y transmisión de enfermedades , Biomédica: Vol. 35 Núm. 2 (2015)
- Dairon Andrés Machado-Agudelo, María Alejandra García, Manuel E. Rueda-Páramo , Nadya Lorena Cardona , Evaluación in vitro de la patogenicidad de los hongos aislados en la región de Urabá (Antioquia, Colombia) contra larvas de Aedes aegypti , Biomédica: Vol. 44 Núm. 4 (2024)
- Yesika del Carmen Rojas, Helena Brochero, Hallazgo de Aedes aegypti (Linnaeus 1762), en el casco urbano del corregimiento de La Pedrera, Amazonas, Colombia , Biomédica: Vol. 28 Núm. 4 (2008)
- María Elena Cuéllar-Jiménez, Olga Lucía Velásquez-Escobar, Ranulfo González-Obando, Carlos Andrés Morales-Reichmann, Detección de Aedes albopictus (Skuse) (Diptera: Culicidae) en la ciudad de Cali, Valle del Cauca, Colombia , Biomédica: Vol. 27 Núm. 2 (2007)
- Gloria Inés Múnera, Jairo Andrés Méndez, Gloria Janneth Rey, Importancia de los análisis serológicos, moleculares y virológicos en la vigilancia de la fiebre amarilla en Colombia, 2006-2008 , Biomédica: Vol. 30 Núm. 3 (2010)
- Natalia Houghton-Triviño, Katherine Martín, Kris Giaya, Jairo A. Rodríguez, Irene Bosch, Jaime E. Castellanos, Comparación de los perfiles de transcripción de pacientes con fiebre de dengue y fiebre hemorrágica por dengue que muestra diferencias en la respuesta inmunitaria y claves en la inmunopatogénesis , Biomédica: Vol. 30 Núm. 4 (2010)
- Berta Nelly Restrepo, Margarita Arboleda, Ruth Ramírez, Gonzalo Álvarez, Actividad sérica de la acetilhidrolasa del factor activador de plaquetas en pacientes afrodescendientes y mestizos con dengue, Colombia , Biomédica: Vol. 31 Núm. 4 (2011)
- Gabriel Parra-Henao, Laura Suárez, Mosquitos (Díptera: Culicidae) vectores potenciales de arbovirus en la región de Urabá, noroccidente de Colombia , Biomédica: Vol. 32 Núm. 2 (2012)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |
Datos de los fondos
-
Secretaría de Educación Superior, Ciencia, Tecnología e Innovación
Números de la subvención PIC-08-IZP-00002

























