Diversidad genética y estructura poblacional de Anopheles triannulatus s.l. en Córdoba, Colombia, determinadas mediante el método de región de código de barras de ADN
Resumen
Introducción. A pesar de los recientes reportes de infección con Plasmodium spp. en poblaciones relacionadas con los linajes noroeste y sureste, Anopheles triannulatus no está incriminado como vector de la transmisión de malaria en Colombia. La diversidad genética puede delimitar la información sobre el flujo génico y la diferenciación poblacional entre localidades con malaria.
Objetivo. Estimar la diversidad genética de An. triannulatus en cinco municipios con alta y baja incidencia de malaria en el departamento de Córdoba.
Materiales y métodos. La recolección entomológica se hizo entre agosto y noviembre de 2016 en los municipios de Tierralta, Puerto Libertador, Montelíbano, Sahagún y Planeta Rica. Como marcador genético, se utilizó la región de código de barras de ADN del gen mitocondrial COI. El análisis genético incluyó la estimación de los parámetros de diversidad haplotípica, estructura genética y flujo génico, la prueba D de neutralidad de Tajima, la red de haplotipos y las relaciones filogenéticas.
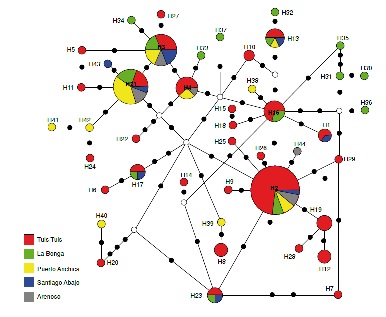
Resultados. Se obtuvieron 148 secuencias parciales de 655 nucleótidos del gen COI, de los cuales se derivaron 44 haplotipos. Los haplotipos H2 y H21 fueron los más frecuentes en las poblaciones. Los valores de la prueba D de Tajima fueron negativos y no significativos (p>0,10). Los estimadores de estructura genética (FST=0,01427) y de flujo génico (Nm=17,27) evidenciaron que no hubo diferenciación genética en las poblaciones muestreadas debido al importante intercambio de migrantes. Mediante
las inferencias filogenéticas y la red de haplotipos, se identificó una sola especie sin diferenciación geográfica o de linajes en el rango geográfico estudiado.
Conclusión. La diversidad genética calculada para An. triannulatus en este contexto, indicó que las poblaciones están en un intercambio constante.
Descargas
Referencias bibliográficas
Walter Reed Biosystematics Unit. Systematic catalog of Culicidae, 2017. Fecha de consulta: 16 de marzo de 2018. Disponible en: http://www.mosquitocatalog.org
Faran M, Linthicum K. A handbook of the Amazonian species of Anopheles (Nyssorhynchus) (Diptera: Culicidae). Mosq Syst. 1981;13:1-81.
Chadde DD, Wilkerson R. Anopheles triannulatus (Neiva and Pinto): A new Anopheles record from Trinidad, West Indies. J Am Mosq Control Assoc. 2005;21:316-7. https://doi.org/10.2987/8756-971X(2005)21[316:ATNAPA]2.0.CO;2
González R, Carrejo N. Introducción al estudio taxonómico de Anopheles de Colombia: claves y notas de distribución. Segunda edicion. Cali: Universidad del Valle; 2009. p. 260.
Sinka M, Rubio-Palis Y, Manguin S, Patil A, Temperley W, Gething P, et al. The dominant Anopheles vectors of human malaria in the Americas: Occurrence data, distribution maps and bionomic précis. Parasit Vectors. 2010;3:72. https://doi.org/10.1186/1756-3305-3-72
Galardo AK, Arruda M, Couto AR, Wirtz R, Lounibos LP, Zimmerman RH. Malaria vector incrimination in three rural riverine villages in the Brazilian Amazon. Am J Trop Med Hyg. 2007;76:461-9. https://doi.org/10.4269/ajtmh.2007.76.461
Tadei WP, Thatcher BD. Malaria vectors in the Brazilian Amazon: Anopheles of the subgenus Nyssorhynchus. Rev Inst Med Trop São Paulo. 2000;42:87-94. https://doi.org/10.1590/S0036-46652000000200005
de Oliveira-Ferreira J, Lourenco-de-Oliveira R, Teva A, Deane LM, Daniel-Ribeiro CT. Natural malaria infections in Anophelines in Rondania State, Brazilian Amazon. Am J Trop Med Hyg. 1990;43:6-10.
Aramburú J, Ramal C, Witzig R. Malaria reemergence in the Peruvian Amazon Region. Emerg Infect Dis. 1999;5:209-15. https://doi.org/10.3201/eid0502.990204
Naranjo-Díaz N, Rosero DA, Rúa-Uribe G, Luckhart S, Correa MM. Abundance, behavior and entomological inoculation rates of anthropophilic anophelines from a primary Colombian malaria endemic area. Parasit Vectors. 2013;6:1-11. https://doi.org/10.1186/1756-3305-6-61
Rosero DN, Naranjo-Díaz N, Álvarez A, Cienfuegos C, Torres S, Luckhart S, et al. Colombian Anopheles triannulatus (Diptera: Culicidae) naturally infected with Plasmodium spp. ISRN Parasitol. 2013:2013:927453.https://doi.org/10.5402/2013/927453
Rosa-Freitas MG, Lourenço-de-Oliveira R, de Carvalho-Pinto CJ, Flores-Mendoza C, Fernandes T, Do-Nascimiento S. Anopheline species complexes in Brazil. Current knowledge of those related to malaria transmission. Mem Inst Oswaldo Cruz. 1998;93:651-5. https://doi.org/10.1590/S0074-02761998000500016
Silva-do-Nacimiento T, Lourenço-de-Oliveira R. Anopheles halophylus, a new species of the Subgenus Nyssorhynchus (Diptera: Culicidae) from Brazil. Mem Inst Oswaldo Cruz. 2002;97:801-11. https://doi.org/10.1590/S0074-02762002000600010
Rosa-Freitas MG, Tsouris P, Peterson AT, Honório NA, Barros FS, Aguiar DB, et al. An ecoregional classification for the state of Roraima, Brazil. The importance of landscape in malaria biology. Mem Inst Oswaldo Cruz. 2007;102:349-57. https://doi.org/10.1590/S0074-02762007005000052
Silva-do-Nascimento TF, Wilkerson RC, Monteiro FA. Molecular confirmation of the specific status of Anopheles halophylus (Diptera: Culicidae) and evidence of a new cryptic species within An. triannulatus in Central Brazil. J Med Entomol. 2006;43:455-9.
Silva-do-Nascimento TF, Damazio L, Pitaluga R, Peixoto AA, Lourenço-de-Oliveira R. Molecular divergence in the timeless and cpr genes among three sympatric cryptic species of the Anopheles triannulatus complex. Mem Inst Oswaldo Cruz. 2011;106:218-22. https://doi.org/10.1590/S0074-02762011000900027
Brochero H, Pareja PX, Ortiz G, Olano VA. Sitios de cría y actividad de picadura de especies de Anopheles en el municipio de Cimitarra, Santander, Colombia. Biomédica. 2006;26:269-77. https://doi.org/10.7705/biomedica.v26i2.1416
Gutiérrez LA, González JJ, Gómez GF, Castro MI, Rosero DA, Luckhart S, et al. Species composition and natural infectivity of anthropophilic Anopheles (Diptera: Culicidae) in Córdoba and Antioquia states in northwestern Colombia. Mem Inst Oswaldo Cruz. 2009;104:1117-24. https://doi.org/10.1590/S0074-02762009000800008
Gutiérrez LA, Naranjo NJ, Cienfuegos AV, Muskus CE, Luckhart S, Conn JE, et al. Population structure analyses and demographic history of the malaria vector Anopheles albimanus from the Caribbean and the Pacific regions of Colombia. Malar J. 2009;8:259. https://doi.org/10.1186/1475-2875-8-259
Rodríguez M, Pérez L, Caicedo JC, Prieto G, Arroyo JA, Kaur H, et al. Composition and biting activity of Anopheles (Diptera: Culicidae) in the Amazon Region of Colombia. J Med Entomol. 2009;46:307-15.
Rosero DA, Jaramillo LM, Gutiérrez LA, Conn JE, Correa MM. Genetic diversity of Anopheles triannulatus s.l. (Diptera: Culicidae) from Northwestern and Southeastern Colombia. Am J Trop Med Hyg. 2012;87:910-20. https://doi.org/10.4269/ajtmh.2012.12-0285
Collins FH, Méndez A, Rasmussen MO, Mehaffey PC, Besansky NJ, Finnerty V. Ribosomal RNA gene probe differentiates member species of the Anopheles gambiae complex. Am J Trop Med Hyg. 1987;37:37-41. https://doi.org/10.4269/ajtmh.1987.37.37
Atencia M, Pérez M, Jaramillo M, Caldera S, Bejarano E. Primer reporte de la mutación F1534C asociada con resistencia cruzada a DDT y piretroides en Aedes aegypti en Colombia. Biomédica. 2016;36:432-7. https://doi.org/10.7705/biomedica.v36i3.2834
Folmer O, Black M, Hoeh W, Lutz R, Vrijenhoek R. DNA primers for amplification of mitochondrial cytochrome c oxidase subunit I from diverse metazoan invertebrates. Mol Mar Biol Biotechnol. 1994;3:294-9.
Kumar S, Stecher G, Tamura K. MEGA7: Molecular evolutionary genetics analysis version 7.0 for bigger datasets. Mol Biol Evol. 2016;33:1870-4. https://doi.org/10.1093/molbev/msw054
Thompson J, Higgins D, Gibson T. CLUSTAL W: Improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice. Nucleic Acids Res. 1994;22:4673-80.
Altschup S, Gish W, Miller W, Myers E, Lipman D. Basic local alignment search tool department of computer science. J Mol Biol. 1990;215:403-10. https://doi.org/10.1016/S0022-2836(05)80360-2
Ratnasingham S, Hebert PDN. Bold: The Barcode of Life Data System (http://www.barcodinglife.org). Molecular Ecology Notes. 2007;7:355-64. https://doi.org/10.1111/j.1471-8286.2007.01678.x
Librado P, Rozas J. DnaSP v5: A software for comprehensive analysis of DNA polymorphism data. Bioinformatics. 2009;25:1451-2. https://doi.org/10.1093/bioinformatics/btp187
Excoffier L, Lischer HE. Arlequin Suite ver 3.5: A new series of programs to perform population genetics analyses under Linux and Windows. Mol Ecol Resour. 2010;10:564-7. https://doi.org/10.1111/j.1755-0998.2010.02847.x
Fluxus Technology. Network 5.0. Clare: Fluxus Technology Ltd.; 2017.
Badelt H, Forster P, Rohl A. Median-joining networks for inferring intraspecific phylogenies. Mol Biol Evol. 1999;16:37-48. https://doi.org/10.1093/oxfordjournals.molbev.a026036
Posada D. jModelTest: Phylogenetic model averaging. Mol Biol Evol. 2008;25:1253-6. https://doi.org/10.1093/molbev/msn083
Ronquist F, Huelsenbeck J. MrBayes 3: Bayesian phylogenetic inference under mixed models. Bioinformatics. 2003;19:1572-4. https://doi.org/10.1093/bioinformatics/btg180
Gutiérrez LA, Gómez GF, González JJ, Castro MI, Luckhart S, Conn JE, et al. Microgeographic genetic variation of the malaria vector Anopheles darlingi Root (Diptera: Culicidae) from Córdoba and Antioquia, Colombia. Am J Trop Med Hyg. 2010;83:38-47. https://doi.org/10.4269/ajtmh.2010.09-0381
Jaramillo LM, Gutiérrez LA, Luckhart S, Conn JE, Correa MM. Molecular evidence for a single taxon, Anopheles nuneztovari s.l., from two endemic malaria regions in Colombia. Mem Inst Oswaldo Cruz. 2011;106:1017-23. https://doi.org/10.1590/S0074-02762011000800020
Pedro PM, Uezu A, Sallum MA. Concordant phylogeographies of 2 malaria vectors attest to common spatial and demographic histories. J Hered. 2010;101:618-27. https://doi.org/10.1093/jhered/esq054
Urrea PA, Correa M, Naranjo-Díaz N. Variabilidad genética de Anopheles punctimacula s.l. en dos localidades de la zona endémica para la malaria: el Bajo Cauca y Alto Sinú. Hechos Microbiológicos. 2014;5:51-62.
Dai Y, Huang X, Cheng P, Liu L, Wang H, Wang H, et al. Development of insecticide resistance in malaria vector Anopheles sinensis populations from Shandong province in China. Malar J. 2015;14:62. https://doi.org/10.1186/s12936-015-0592-8
Scarpassa VM, Cunha-Machado AS, Saraiva JF. Evidence of new species for malaria vector Anopheles nuneztovari sensu lato in the Brazilian Amazon region. Malar J. 2016;15:205. https://doi.org/10.1186/s12936-016-1217-6
McKeon SN, Lehr M, Wilkerson RC, Ruiz JF, Sallum M, Lima JB, et al. Lineage divergence detected in the malaria vector Anopheles marajoara (Diptera: Culicidae) in Amazonian Brazil. Malar J. 2010;9:271. https://doi.org/10.1186/1475-2875-9-271
Ahumada ML, Orjuela LI, Pareja PX, Conde M, Cabarcas DM, Cubillos EFG, et al. Spatial distributions of Anopheles species in relation to malaria incidence at 70 localities in the highly endemic Northwest and South Pacific coast regions of Colombia. Malar J. 2016;15:407. https://doi.org/10.1590/S0074-02762009000800008
Algunos artículos similares:
- Juan J. Yunis, Luis E. Acevedo, David S. Campo, Emilio J. Yunis, Origen geno-geográfico de haplotipos STR del cromosoma Y en una muestra caucásico-mestiza y afrodescendiente de Colombia , Biomédica: Vol. 33 Núm. 3 (2013)
- Liliana Santacoloma, Tania Tibaduiza, Marcela Gutiérrrez, Helena Brochero, Sensibilidad de Anopheles darlingi Root 1840 a insecticidas, en dos localidades de los departamentos de Santander y Caquetá, Colombia , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Jorge A. Vega, Simón Villegas-Ospina, Wbeimar Aguilar-Jiménez, María T. Rugeles, Gabriel Bedoya, Wildeman Zapata, Los haplotipos en CCR5-CCR2, CCL3 y CCL5 se asocian con resistencia natural a la infección por el HIV-1 en una cohorte colombiana , Biomédica: Vol. 37 Núm. 2 (2017)
- Lorena I. Orjuela, Manuela Herrera, Holmes Erazo, Martha L. Quiñones, Especies de Anopheles presentes en el departamento del Putumayo y su infección natural con Plasmodium , Biomédica: Vol. 33 Núm. 1 (2013)
- Helena Brochero, Paula Ximena Pareja, Gloria Ortiz, Víctor Alberto Olano, Sitios de cría y actividad de picadura de especies de anopheles en el municipio de Cimitarra, Santander, Colombia. , Biomédica: Vol. 26 Núm. 2 (2006)
- Pilar Jiménez, Jan E. Conn, Robert Wirtz, Helena Brochero, Anopheles (Díptera: Culicidae) vectores de malaria en el municipio de Puerto Carreño, Vichada, Colombia , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Dora Amparo Estrada, Martha L. Quiñoes, Diana Maria Sierra, David A. Calle, Fredy Ruiz, Holmes F. Erazo, Yvonne Marie Linton, Utilidad de la morfología de los huevos como un método indirecto para identificar Anopheles benarrochi Gabaldón,Cova García & López, Anopheles oswaldoi (Peryassu) y Anopheles rangeli Gabaldón, Cova García & López, (Diptera:Culicidae) en Putumayo, Colombia. , Biomédica: Vol. 23 Núm. 4 (2003)
- Elizabeth Borrero, Gabriel Carrasquilla, Neal Alexander, Descentralización y reforma: ¿cuál es su impacto sobre la incidencia de malaria en los municipios colombianos? , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Gabriel Bedoya, Jenny García, Patricia Montoya, Winston Rojas, Maria Eugenia Amézquita, Iván Soto, Maria Cecilia López, Jorge Ospina-Duque, Andrés Ruiz-Linares, Análisis de isonimia entre poblaciones del noroeste de Colombia , Biomédica: Vol. 26 Núm. 4 (2006)
- Alejandro Silva, Ignacio Briceño, Javier Burgos, Diana Torres, Victoria Villegas, Alberto Gómez, Jaime Eduardo Bernal, Análisis de ADN mitocondrial en una muestra de restos óseos arcaicos del periodo Herrera en la sabana de Bogotá , Biomédica: Vol. 28 Núm. 4 (2008)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























