Asociación de variantes polimorfas de los genes PTPN22, TNF y VDR en niños con nefritis lúpica: un estudio de tríos en familias colombianas
Resumen
Introducción. El lupus eritematoso sistémico es una enfermedad autoinmunitaria cuya gravedad varía según la raza, el sexo y la edad de aparición. Esta disparidad también se observa en los marcadores genéticos asociados con la enfermedad presentes en los genes PTPN22, VDR y TNF. La estratificación genética que presentan las diferentes poblaciones en el mundo puede influir en dicha variabilidad.
Objetivo. Analizar la asociación de variantes genéticas de los genes PTPN22, VDR y TNF con nefritis lúpica en niños y su caracter de hereditarias en familias colombianas.
Materiales y métodos. Se llevó a cabo un estudio basado en familias con 46 tríos (caso, padre y madre). Se hizo la genotipificación de las variantes rs2476601 de PTPN22, rs361525 y rs1800629 del TNF, y TaqI [rs731236], ApaI [rs7975232], BsmI [rs1544410] y FokI [rs2228570] del VDR, mediante reacción en cadena de la polimerasa cuantitativa (quantitative Polymerase Chain Reaction, qPCR). Se estimó el efecto de la transmisión del alelo de riesgo de padres a hijos y el desequilibrio de ligamiento de los loci VDR y TNF.
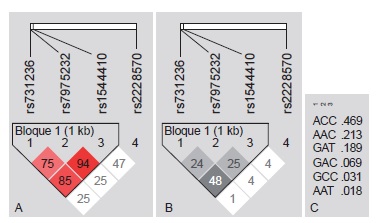
Resultados. Se observó que el alelo A de rs2476601 en PTPN22 se distribuyó en 8,69 % (n=16) de los padres y en 19,5 % (n=18) de los casos, y que su transmisión de padres a hijos fue 17 veces mayor con relación al alelo G (p=0,028). Los polimorfismos de TNF y VDR no presentaron desequilibrio de transmisión. Las variantes TaqI, ApaI y BsmI del VDR presentaron desequilibrio de ligamiento.
Conclusión. Estos hallazgos evidenciaron una asociación del polimorfismo rs2476601 de PTPN22 con la nefritis lúpica en niños, determinada por su transmisión en el grupo de familias estudiadas.
Descargas
Referencias bibliográficas
Bonanni A, Vaglio A, Bruschi M, Sinico RA, Cavagna L, Moroni G, et al. Multi-antibody composition in lupus nephritis: Isotype and antigen specificity make the difference. Autoimmun Rev. 2015;14:692-702. http://dx.doi.org/10.1016/j.autrev.2015.04.004
Mohan C, Putterman C. Genetics and pathogenesis of systemic lupus erythematosus and lupus nephritis. Nat Rev Nephrol. 2015;11:329-41. http://dx.doi.org/10.1038/nrneph.2015.33
Pons-Estel BA, Catoggio LJ, Cardiel MH, Soriano ER, Gentiletti S, Villa AR, et al. The GLADEL multinational Latin American prospective inception cohort of 1,214 patients with systemic lupus erythematosus: Ethnic and disease heterogeneity among “Hispanics”. Medicine (Baltimore). 2004;83:1-17. http://dx.doi.org/10.1097/01.md.0000104742.42401.e2
Ramírez-Gómez LA, Uribe-Uribe O, Osio-Uribe O, Grisales-Romero H, Cardiel MH, Wojdyla D, et al. Childhood systemic lupus erythematosus in Latin America. The GLADEL experience in 230 children. Lupus. 2008;17:596-604. http://dx.doi.org/10.1177/0961203307088006
Makashir SB, Kottyan LC, Weirauch MT. Meta-analysis of differential gene co-expression: Application to lupus. Pac Symp Biocomput. 2015:443-54. http://dx.doi.org/10.1142/9789814644730_0042
Dema B, Charles N. Advances in mechanisms of systemic lupus erythematosus. Discov Med. 2014;17:247-55.
Kunz M. Lupus erythematosus. Part I: Epidemiology, genetics and immunology. J Dtsch Dermatol Ges. 2013;11:709-19. http://dx.doi.org/10.1111/ddg.12165
Sinha R, Raut S. Pediatric lupus nephritis: Management update. World J Nephrol. 2014;3:16-23. http://dx.doi.org/10.5527/wjn.v3.i2.16
Ortega LM, Schultz DR, Lenz O, Pardo V, Contreras GN. Review: Lupus nephritis: Pathologic features, epidemiology and a guide to therapeutic decisions. Lupus. 2010;19:557-74. http://dx.doi.org/10.1177/0961203309358187
Shi L, Wei Y, Xun W, Han D. Meta-analysis of the correlation between PTPN22 gene polymorphisms and susceptibility to systemic lupus erythematosus. Asia Pac J Public Health. 2013;25(Suppl.4):22S-9. http://dx.doi.org/10.1177/1010539513496268
Ramírez M, Quintana G, Díaz-Gallo LM, Caminos J, Garcés M, Cepeda L, et al. The PTPN22 C1858T variant as a risk factor for rheumatoid arthritis and systemic lupus erythematosus but not for systemic sclerosis in the Colombian population. Clin Exp Rheumatol. 2012;30:520-4.
Hu W, Niu G, Lin Y, Chen X, Lin L. Impact of the polymorphism in vitamin D receptor gene BsmI and the risk of systemic lupus erythematosus: An updated metaanalysis. Clin Rheumatol. 2015;35:927-34. http://dx.doi.org/10.1007/s10067-015-3157-x
Mao S, Huang S. Association between vitamin D receptor gene BsmI, FokI, ApaI and TaqI polymorphisms and the risk of systemic lupus erythematosus: A meta-analysis. Rheumatol Int. 2014;34:381-8. http://dx.doi.org/10.1007/s00296-013-2898-6
Pan HF, Leng RX, Wang C, Qin WZ, Chen LL, Zha ZQ, et al. Association of TNF-alpha promoter-308 A/G polymorphism with susceptibility to systemic lupus erythematosus: A metaanalysis. Rheumatol Int. 2012;32:2083-92. http://dx.doi.org/10.1007/s00296-011-1924-9
Zou YF, Feng XL, Pan FM, Su H, Tao JH, Ye DQ. Metaanalysis of TNF-alpha promoter - 238A/G polymorphism and SLE susceptibility. Autoimmunity. 2010;43:264-74.
http://dx.doi.org/10.3109/08916930903509049
Niu Z, Zhang P, Tong Y. Value of HLA-DR genotype in systemic lupus erythematosus and lupus nephritis: A metaanalysis. Int J Rheum Dis. 2015;18:17-28. http://dx.doi.org/10.1111/1756-185X.12528
Pan CF, Wu CJ, Chen HH, Dang CW, Chang FM, Liu HF, et al. Molecular analysis of HLA-DRB1 allelic associations with systemic lupus erythematous and lupus nephritis in Taiwan. Lupus. 2009;18:698-704. http://dx.doi.org/10.1177/0961203308101955
Ghodke-Puranik Y, Niewold TB. Immunogenetics of systemic lupus erythematosus: A comprehensive review. J Autoimmun. 2015;64:125-36. http://dx.doi.org/10.1016/j.jaut.2015.08.004
Lewis CM. Genetic association studies: Design, analysis and interpretation. Brief Bioinform. 2002;3:146-53. http://dx.doi.org/10.1093/bib/3.2.146
Campbell H, Rudan I. Interpretation of genetic association studies in complex disease. Pharmacogenomics J. 2002;2:349-60. http://dx.doi.org/10.1038/sj.tpj.6500132
Robinson MR, Wray NR, Visscher PM. Explaining additional genetic variation in complex traits. Trends Genet. 2014;30124-32. http://dx.doi.org/10.1016/j.tig.2014.02.003
Kaufman JS, Cooper RS. Commentary: Considerations for use of racial/ethnic classification in etiologic research. Am J Epidemiol. 2001;154:291-8. http://dx.doi.org/0.1093/aje/154.4.291
Jenkins JM, McGowan P, Knafo-Noam A. Parentoffspring transaction: Mechanisms and the value of within family designs. Horm Behav. 2016;77:53-61. http://dx.doi.org/10.1016/j.yhbeh.2015.06.018
Infante-Rivard C, Mirea L, Bull SB. Combining case control and case-trio data from the same population in genetic association analyses: Overview of approaches and illustration with a candidate gene study. Am J Epidemiol.2009;170:657-64. http://dx.doi.org/10.1093/aje/kwp180
Santos JL, Pérez F, Carrasco E, Albala C. Uso de tríos caso-padres en estudios epidemiológicos de asociación entre polimorfismos genéticos y enfermedades complejas. Rev Med Chil. 2002;130:1307-15. http://dx.doi.org/10.4067/S0034-98872002001100016
Guo W, Fung WK. Combining the case-control methodology with the small size transmission/disequilibrium test for multiallelic markers. Eur J Hum Genet. 2005;13:1007-12. http://dx.doi.org/10.1038/sj.ejhg.5201453
Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 1997;40:1725. http://dx.doi.org/10.1002/1529-0131(199709)40:9<1725::AIDART29>3.0.CO;2-Y
Miller SA, Dykes DD, Polesky HF. A simple salting out procedure for extracting DNA from human nucleated cells. Nucleic Acids Res. 1988;16:1215. http://dx.doi.org/10.1093/nar/16.3.1215
Laird NM, Lange C. Family-based designs in the age of large-scale gene-association studies. Nat Rev Genet. 2006;7:385-94. http://dx.doi.org/10.1038/nrg1839
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























